ЧАСТЬ ВТОРАЯ. НАУКА О СЛОЖНОСТИ
Глава 4. ЭНЕРГИЯ И ИНДУСТРИАЛЬНЫЙ ВЕК
1. Тепло — соперник гравитации
Ignis mutat res. Это высказывание, известное с незапамятных времен, всегда связывало химию с «наукой об огне». В XVIII в., начиная с концептуальной перестройки, вынудившей науку пересмотреть то, что ранее отвергалось ею во имя механистического мировоззрения, а именно такие понятия, как «необратимость» и «сложность», огонь стал частью экспериментальной науки.
Огонь преобразует материю. Он приводит к химическим реакциям, к таким процессам, как плавление и испарение. Огонь заставляет топливо сгорать и высвобождать тепло. Из всех этих общеизвестных фактов наука XIX в. сосредоточила внимание на одном; горение сопровождается выделением тепла, а подвод тепла может вызывать увеличение объема, в результате чего горение совершает работу. Таким образом, огонь приводит к созданию машины нового типа — тепловой машины, — технологическому новшеству, ставшему основой индустриального общества1.
Интересно отметить, что Адам Смит работал над своим «Исследованием о природе и причинах богатства народов» и собирал данные о перспективах и определяющих факторах роста промышленности в том самом университете, в стенах которого Джеймс Уатт завершал доводку своей паровой машины. Тем не менее Адам Смит смог найти для каменного угля единственно полезное применение — как источник тепла. (В XVIII в. еще не были известны другие источники энергии, кроме воды, ветра, мускульной силы животных и приводимых ими в движение простейших машин.)
Быстрое распространение британской паровой машины вызвало новый интерес к механическому действию теплоты, и термодинамика, детище этого интереса, занималась не столько выяснением природы тепла, сколько скрытыми в тепле возможностями производства «механической энергии».
Что же касается рождения «науки о сложности», то мы предлагаем датировать его 1811 годом, когда барону Жан-Батисту Жозефу Фурье, префекту Изера, была присуждена премия Французской академии наук за математическую теорию распространения тепла в твердых телах.
Установленный Фурье результат был удивительно прост и изящен: поток тепла пропорционален градиенту температуры. Замечательно, что этот простой закон применим к веществу, в каком бы состоянии оно ни находилось: твердом, жидком или газообразном. Кроме того, закон Фурье выполняется независимо от химического состава тела, будь оно из золота или из железа. Специфическим для каждого вещества является коэффициент пропорциональности между тепловым потоком и градиентом температуры.
Ясно, что универсальный характер закона Фурье не связан непосредственно с динамическими взаимодействиями, описываемыми законом Ньютона, поэтому формулировку закона теплопроводности можно рассматривать как исходную точку науки нового типа. Действительно, простота предложенного Фурье математического описания распространения тепла разительно контрастирует со сложностью вещества, рассматриваемого с точки зрения его молекулярного строения. Твердое тело, газ или жидкость представляют собой макроскопические системы, состоящие из огромного числа молекул, и тем не менее теплопроводность описывается одним-единственным законом. Фурье вывел свой закон в то время, когда в европейской науке школа Лапласа занимала господствующее положение. Лаплас, Лагранж и их ученики пытались объединенными усилиями критиковать теорию Фурье, но были вынуждены отступить2. Сбывшаяся было мечта Лапласа потерпела первое поражение. Фурье создал физическую теорию, не уступавшую по математической строгости механическим законам движения, но в то же время остававшуюся совершенно чуждой ньютоновскому миру. С момента появления теории теплопроводности Фурье математика, физика и ньютоновская наука перестали быть синонимами.
Открытие закона теплопроводности имело непреходящее значение. Интересно отметить, что с появлением закона Фурье исторические пути развития физики во Франции и Англии разошлись и к современному этапу французские физики и их английские коллеги следовали различными маршрутами.
Во Франции крушение мечты Лапласа привело к позитивистской классификации науки на иерархически упорядоченные отделы, предложенные Огюстом Контом. Контовская классификация науки была подробно проанализирована Мишелем Серром3. В физике сосуществуют две универсалии: тепло и гравитация. Более того, как вынужден признать позднее Конт, эти две универсалии — антагонисты. Гравитация действует на инертную массу, которая подчиняется гравитации, не испытывая ее действия иным путем, кроме как через движение, которое приобретает или передает. Тепло преобразует вещество, определяет изменения состояния и вызывает изменения внутренних свойств. В некотором смысле это было подтверждением протеста химиков-антиньютонианцев и всех тех, кто подчеркивал различие между чисто пространственно-временным поведением, приписываемым массе, и специфической активностью вещества. Именно такое различие и было принято за основу классификации наук, проведенной Контом по общему признаку — порядку, т. е. равновесию. К механическому равновесию сил позитивистская классификация просто добавила понятие теплового равновесия.
С другой стороны, в Британии с появлением теории распространения тепла отнюдь не прекратились попытки объединения всех областей знания, более того, там наметилось новое направление научных исследований — первые шаги в создании теории необратимых процессов.
Закон Фурье, если его применить к изолированному телу с неоднородным распределением температуры, описывает постепенное установление равновесия. Теплопроводность приводит к все большему выравниванию распределения температуры до тех пор, пока распределение во всем теле не станет однородным. Всякий знает, что выравнивание температуры — процесс необратимый. Еще столетие назад Берхаве подчеркивал, что тепло всегда распространяется и выравнивается. Таким образом, наука о сложных явлениях (основанных на взаимодействии большого числа частиц) и временная асимметрия с самого начала оказались взаимосвязанными. Но теплопроводность стала исходным пунктом исследований природы необратимости не раньше, чем была установлена ее связь с понятием «диссипация», рассматриваемым с инженерной точки зрения4.
Познакомимся несколько подробнее со структурой новой «науки о тепле» в том виде, в каком она сложилась в начале XIX в. Подобно механике, наука о тепле включала в себя и оригинальную концепцию физического объекта, и определение машины, или двигателя, т. е. отождествление причины и следствия в специфическом способе производства механической работы.
При исследовании физических процессов, связанных с теплом, состояние системы необходимо задавать, указывая не положения и скорости ее составных частей (в объеме газа порядка 1 см3 содержится около 1023 молекул), как в случае динамики, а некоторую совокупность макроскопических параметров, таких, как температура, давление, объем и т. д. Кроме того, необходимо учитывать граничные условия, описывающие отношение системы к окружающей среде.
В качестве примера рассмотрим одно из характерных свойств макроскопической системы — ее удельную теплоемкость. Напомним, что удельной теплоемкостью называется количество тепла, которое необходимо сообщить системе, чтобы поднять ее температуру на один градус при постоянном объеме или давлении. Чтобы исследовать удельную теплоемкость (например, при постоянном объеме), систему необходимо привести во взаимодействие с окружающей средой: система должна получить определенное количество тепла, в то время как объем ее поддерживается постоянным, а температура может изменяться.
В более общем случае систему можно подвергнуть механическому воздействию (например, поддерживать постоянство давления или объема с помощью поршня), тепловому воздействию (подводить к системе или отводить от нее некоторое количество тепла) или химическому воздействию (создавать поток реагирующих веществ и продуктов реакции между системой и окружающей средой). Как мы уже упоминали, давление, объем, химический состав и температура являются классическими физико-химическими параметрами, через которые выражаются свойства макроскопических систем. Термодинамику можно определить как науку о корреляции между изменениями этих свойств. Следовательно, термодинамические объекты приводят к новой по сравнению с динамическими объектами точке зрения. Цель теории состоит не в предсказании поведения системы в терминах взаимодействия частиц, а в предсказании реакции системы на изменения, вводимые нами извне.
Механическое устройство (машина) возвращает в виде работы потенциальную энергию, полученную им из внешнего мира. Причина и следствие имеют одинаковую природу и, по крайней мере в идеальном случае, эквивалентны. Действие тепловой машины, в отличие от механического устройства, сопряжено с материальными изменениями состояний, включающими преобразование механических свойств системы, расширением и увеличением объема. Производимую тепловым двигателем работу следует рассматривать как результат подлинного процесса преобразования, а не только передачи движения. Таким образом, тепловая машина — не пассивное устройство. Строго говоря, она производит движение. С этой особенностью тепловой машины связана новая проблема: чтобы восстановить способность системы производить движение, ее необходимо возвратить в начальное состояние. Следовательно, необходим второй процесс, второе изменение состояния, которое компенсировало бы то изменение, которое производит движение. В тепловой машине таким вторым процессом, противоположным первому, является охлаждение системы до начальных значений температуры, давления и объема.
Понятие необратимого процесса было введено в физику в связи с проблемой повышения коэффициента полезного действия (кпд) тепловых машин, т. е. отношения между производимом работой и теплом, которое необходимо подвести к системе, чтобы осуществить два взаимно компенсирующих, процесса. Мы еще вернемся к вопросу о значении закона Фурье для этой проблемы, но сначала опишем ту существенную роль, которую играет закон сохранения энергии.
2. Принцип сохранения энергии
Мы уже отмечали, что в классической динамике энергия занимает центральное место. Гамильтониан (сумму кинетической и потенциальной энергий) можно представить в канонических переменных — координатах и импульсах. В процессе движения значения канонических переменных изменяются, значение же гамильтониана остается постоянным. Динамическое изменение лишь перераспределяет относительную значимость потенциальной и кинетической энергий, оставляя неизменной их сумму.
Начало XIX в. совпало с бурным периодом в истории экспериментальной физики5. Нескончаемая вереница открытий показала физикам, что движение способно порождать не только изменения в относительных положениях тел в пространстве. Новые процессы, открытые в лабораториях, постепенно создали сеть, связавшую воедино все новые области физики с другими более традиционными областями, например с механикой. Одну из таких связей неожиданно обнаружил Гальвани. До него были известны только статические электрические заряды. Производя опыты с препаратами лапок лягушек, Гальвани впервые экспериментально наблюдал действие электрического тока. А. Вольта вскоре понял, что «гальванические» сокращения лапок лягушки вызывает проходящий через них электрический ток. В 1800 г. Вольта построил химическую батарею: стало возможным получать электричество с помощью химических реакций. Затем был открыт электролиз: электрический ток позволял изменять химическое сродство и проводить химические реакции. Но электрический ток давал также свет и тепло, а в 1820 г. Эрстед обнаружил, что электрический ток оказывает действие и на магнитную стрелку. В 1822 г. Зеебек показал, что тепло может быть источником электричества, а в 1834 г. им был открыт способ охлаждения вещества с помощью электричества. В 1831 г. Фарадей индуцировал электрический ток с помощью магнитных эффектов. Так постепенно была открыта целая совокупность новых физических эффектов. Естественнонаучный горизонт расширялся с неслыханной быстротой.
Решающий шаг был сделан в 1847 г. Джоулем: он понял, что связи, обнаруженные между выделением или поглощением тепла, электричеством и магнетизмом, протеканием химических реакций, а также биологическими объектами, носят характер «превращения». Идея превращения, опирающаяся на постулат о количественном сохранении «чего-то» при его качественных изменениях, обобщает то, что происходит при механическом движении. Как мы уже знаем, полная энергия сохраняется, в то время как потенциальная энергия переходит, превращается в кинетическую, и наоборот. Джоуль определил общий эквивалент для физико-химических трансформаций, что позволило измерить сохраняющуюся величину. Впоследствии6 эта величина стала известна как «энергия». Джоуль установил первую эквивалентность, измерив механическую работу, которую необходимо затратить, чтобы поднять температуру данного количества воды на один градус. Так среди ошеломляющего потока новых разнообразных открытий был обнаружен унифицирующий элемент. Сохранение энергии при самых различных преобразованиях, претерпеваемых физическими, химическими и биологическими системами, стало путеводным принципом в исследовании новых процессов.
Неудивительно, что закон сохранения энергии был столь важен для физиков XIX в. Для многих из них он был воплощением единства природы. Это убеждение отчетливо звучит в высказывании Джоуля, выдержанном в традициях английской науки:
«Явления природы, механические, химические или биологические, состоят почти полностью из непрерывного превращения тяготения на расстоянии живой силы [кинетической энергии] в тепло, и наоборот. Тем самым поддерживается порядок во Вселенной: ничто не расстрачивается, ничто не утрачивается, а весь механизм при всей своей сложности работает слаженно и гармонично. И хотя, как в ужасном видении пророка Иезекииля, «казалось, будто колесо находилось в колесе» (Иезек, 1, 16) и все кажется сложным и вовлеченным в хитросплетения почти неисчерпаемого многообразия причин, следствий, превращений и выстраивания в определенной последовательности, тем не менее сохраняется идеальнейший порядок и все бытие послушно непререкаемой воле бога»7.
Еще более показателен случай немецких ученых Гельмгольца, Майера и Либиха. Все трое принадлежали к культурной традиции, которая отвергла бы взгляды Джоуля с позиций чисто позитивистской практики. В ту пору, когда они совершали свои открытия, ни один из них не был, строго говоря, физиком. Однако их всех интересовала физиология дыхания. Со времен Лавуазье это был своего рода эталон проблемы, в которой функционирование живого существа поддавалось описанию в точных физических и химических терминах, таких, как расход кислорода при горении, выделение тепла и мускульная работа. Эта проблема привлекала физиологов и химиков, чуждых чисто умозрительным построениям романтиков и жаждущих внести свой вклад в экспериментальную науку. Обстоятельства, при которых эти трое ученых пришли к заключению, что дыхание, да и природа в целом подчиняются универсальной «эквивалентности», лежащей в основе всех, больших и малых, явлений, позволяют утверждать, что именно немецкой философской традиции открыватели закона сохранения энергии обязаны своей концепцией, совершенно чуждой позитивисткой позиции: все трое без малейших колебаний пришли к выводу о всеобщем характере закона сохранения энергии, о том, что он пронизывает всю природу до мельчайших кирпичиков мироздания.
Особенно замечательным нам представляется случай Майера8. Работая в молодые годы врачом в голландских колониях на Яве, Майер обратил внимание на ярко красный цвет венозной крови у одного из своих пациентов. Это наблюдение привело его к заключению, что жителям жаркого тропического климата требуется меньше кислорода для поддержания нормальной температуры тела, чем в средних широтах, чем и объясняется яркий цвет их крови. Майер продолжил свои исследования и установил баланс между потреблением кислорода, являющимся источником энергии, и потреблением энергии, затрачиваемой на поддержание постоянной температуры тела, несмотря на тепловые потери и мышечную работу. Это была счастливая догадка, так как причиной яркого цвета крови пациента вполне могла быть, например, его «лень». Но Майер не остановился на достигнутом и, продолжив свои рассуждения, пришел к заключению, что баланс потребления кислорода и тепловых потерь — не более чем частное проявление существования какой-то неразрушимой «силы», лежащей в основе всех явлений.
Тенденция видеть в явлениях природы продукты лежащей в их основе реальности, сохраняющей постоянство при всех трансформациях, поразительно напоминает идеи Канта. Влияние Канта отчетливо ощущается и в другой идее, которую разделяли некоторые физиологи: в необходимости различать витализм как философскую спекуляцию и витализм как проблему научной методологии. Для тех физиологов, кто придерживался этой точки зрения, даже если бы существовала «жизненная» сила, лежащая в основе функционирования живых организмов, объект физиологии по своей природе оставался бы чисто физико-химическим. По двум названным выше причинам кантианство, узаконившее ту систематическую форму, которую приняла математическая физика в XVIII в., по праву может считаться одним из источников обновления физики в XIX в.9
Гельмгольц совершенно открыто признавал влияние Канта. Для Гельмгольца закон сохранения энергии был лишь воплощением в физике общего априорного требования, на котором зиждется вся наука, а именно постулата о фундаментальной инвариантности, которая кроется за всеми трансформациями, происходящими в природе:
«Цель указанных* наук заключается в отыскании законов, благодаря которым отдельные процессы в природе могут быть сведены к общим правилам и могут быть снова выведены из этих последних. Эти правила, к которым относятся, например, законы преломления или отражения света, закон Мариотта и Гей-Люссака для объема газов, являются, очевидно, не чем иным, как общим видовым понятием, которым охватываются все относящиеся сюда явления. Разыскание подобных законов является делом экспериментальной части наших наук; теоретическая часть старается в то же время определить неизвестные причины явлений из их видимых действий; она стремится понять их из закона причинности.
Мы вынуждены были так поступать и имеем на это право благодаря основному закону, по которому всякое изменение в природе должно иметь достаточное основание. Ближайшие причины, которым мы подчиняем естественные явления, могут быть в свою очередь неизменными или изменяющимися. В последнем случае тот же закон принуждает нас искать другие причины этого изменения и так далее до тех пор, пока мы не доходим до последних причин, которые действуют по неизменному закону и которые, следовательно, в каждое время при одинаковых условиях вызывают одно и то же действие. Конечной целью теоретического естествознания и является, таким образом, разыскание последних неизменных причин явлений в природе»10.
С появлением закона сохранения энергии начала формироваться идея о новом золотом веке физики, который должен был бы в конечном счете привести к наиболее широкому обобщению механики.
Открытие закона сохранения энергии имело далеко идущие культурные последствия. В их число входило и представление об обществе и человеке как о машинах, преобразующих энергию. Но превращение энергии не может быть конечным звеном цепи. Оно отражает пассивные и управляемые аспекты природы, но за ними должен находиться еще один более «активный» уровень. Ницше был одним из тех, кто уловил эхо актов творения и разрушения, выходящих за рамки одного лишь сохранения или превращения. Результаты, являющиеся различиями, могут порождать только различие, например разность температур или уровней потенциальной энергии11. Превращение энергии есть всего лишь уничтожение одного различия с одновременным созданием другого. Сила природы оказывается, таким образом, скрытой использованием эквивалентностей. Но существует другой аспект природы, имеющий непосредственное отношение к котлам паровых двигателей, химическим превращениям, жизни и смерти и выходящий за рамки эквивалентностей и сохранения энергии12. Говоря об этом аспекте, мы подходим к самому важному вкладу термодинамики в естествознание — понятие необратимости.
3. Тепловые машины и стрела времени
Сравнивая механические устройства с тепловыми машинами, например с паровозными котлами с их раскаленными докрасна топками, мы наглядно видим брешь, отделяющую классический век от технологии XIX в. Тем не менее физики поначалу думали, что эту брешь можно игнорировать, что тепловые машины удастся описывать так же, как некогда механические, пренебрегая тем решающим фактом, что использованное тепловой машиной горючее исчезает навсегда. Но вскоре подобному благодушию пришел конец. Для классической механики символом природы были часы, для индустриального века таким символом стал резервуар энергии, запас которого всегда грозил иссякнуть. Мир горит как огромная печь; энергия, хотя она и сохраняется, непрерывно рассеивается.
Первоначальную формулировку второго начала термодинамики, которая позволила впервые количественно выразить необратимость, предложил в 1824 г. Сади Карно — до того, как Майер (1842) и Гельмгольц (1847) сформулировали в общем виде закон сохранения энергии. Карно, продолжая работу своего отца Лазара Карно, автора весьма авторитетного трактата по теории машин (механических устройств), занимался анализом работы тепловой машины.
При описании механических устройств движение предполагается заданным. На современном языке это соответствует сохранению энергии и импульса. Движение лишь претерпевает превращения и передается другим телам. Но аналогия между механическим устройством и тепловой машиной была естественной для Сади Карно, поскольку он, как и большинство ученых его времени, предполагал, что тепло сохраняется подобно тому, как сохраняется механическая энергия.
Вода, падающая с одного уровня на другой, способна приводить в движение мельничное колесо. Аналогичным образом Сади Карно предположил, что существуют два источника, один из которых отдает тепло системе двигателя, а второй, находящийся при другой температуре, поглощает тепло, отданное первым. Таким образом, работу тепловой машины Сади Карно представил как движение тепла через машину между двумя источниками, находящимися при различных температурах. Иначс говоря, работу, производимую машиной, по Карно, совершает движущая сила огня.
Сади Карно поставил перед собой те же вопросы, какие задавал его отец13. У какой машины коэффициент полезного действия будет наиболее высоким? Каковы источники потерь? При каких процессах тепло распространяется, не производя работы? Лазар Карно пришел к заключению, что для достижения наивысшего коэффициента полезного действия при постройке и эксплуатации механического устройства следует сводить до минимума удары, трение и резкие, скачкообразные изменения скорости, т. е., короче говоря, все, что происходит при внезапном соприкосновении тел, движущихся с различными скоростями. Рассуждая так, Лазар Карно лишь следовал физике своего времени, считавшей, что только непрерывные изменения консервативны, а все скачкообразные изменения движения сопряжены с необратимой потерей «живой силы». Заключение Сади Карно было аналогичным: идеальная тепловая машина вместо того, чтобы избегать любых контактов между телами, движущимися с различными скоростями, должна избегать любых контактов между телами, имеющими различные температуры.
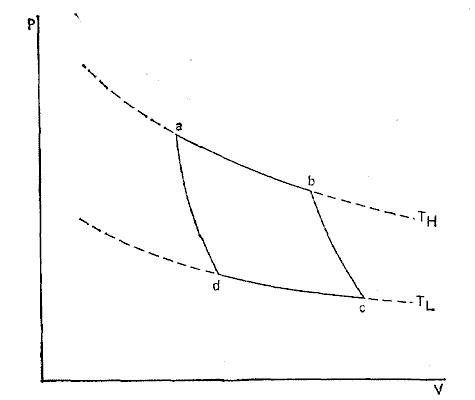 |
Рис. 2. Цикл Карно на диаграмме давление-объем (идеальная тепловая машина, функционирующая между двумя источниками: нагревателем при температуре ТH и холодильником при температуре TL, TH>TL.). При переходе из состояния a в состояние b происходит изотермический процесс: система, температура которой поддерживается равной температуре нагревателя Тн, поглощает тепло и расширяется. При переходе из состояния b в состояние с происходит адиабатический процесс: теплоизолированная система продолжает расширяться и температура понижается с ТH до TL. На этих двух стадиях система производит механическую работу. При переходе из состояния с в состояние d происходит еще один изотермический процесс: система, температура которой поддерживается равной температуре холодильника TL, сжимается и выделяет тепло. При переходе из состояния d в а происходит еще один адиабатический пропесс: теплоизолированная система сжимается и температура ее повышается с TL до ТH.
Следовательно, рассуждал Сади Карио, цикл необходимо строить так, чтобы ни одно изменение температуры не было обусловлено прямым потоком тепла между двумя телами, находящимися при различных температурах. Поскольку такие потоки не производили бы никакой механической работы, они приводили бы только к снижению кпд.
Идеальный цикл Kарно представляет собой, таким образом, весьма хитроумное приспособление, позволяющее достигать парадоксального результата: переноса тепла между двумя источниками, находящимися при различных температурах, без прямого контакта между телами с различной температурой. Цикл Карно подразделяется на четыре стадии. На каждой из двух изотермических стадий система находится в контакте с одним из двух тепловых источников, а ее температура поддерживается равной температуре этого источника. Находясь в контакте с горячим источником (нагревателем), система поглощает тепло и расширяется. Находясь в контакте с холодным источником (холодильником), система теряет тепло и сжимается. Две изотермические стадии связаны между собой двумя стадиями, на которых система изолирована от источников, т. е. тепло не поступает в систему и не покидает ее, но температура системы изменяется в результате соответственно расширения и сжатия. Объем продолжает изменяться до тех нор, пока система не перейдет от температуры одного источника к температуре другого.
Весьма замечательно, что в приведенном выше описании идеальной тепловой машины ни разу не упоминаются лежащие в основе его реализации необратимые процессы. Ни слова не говорится о печи, в которой сгорает уголь. Предложенная Сади Карно модель отражает лишь конечный результат горения: возможность поддержания разности температур между двумя источниками.
В 1850 г. Клаузиус дал новое описание цикла Карно — с точки зрения закона сохранения энергии. Он обнаружил, что необходимость в двух тепловых источниках (нагревателе и холодильнике) и выведенная Карно формула для теоретического кпд отражают проблему, специфическую для тепловых машин: необходимость процесса, компенсирующего превращение (в случае цикла Карно — охлаждение в контакте с источником, находящимся при более низкой температуре), для того чтобы вернуть машину к начальным механическим и тепловым условиям. Соотношения баланса, выражающие превращения энергии, оказались теперь объединенными новыми отношениями эквивалентности между воздействиями двух процессов — потока тепла между источниками и превращения тепла в работу — на состояние системы. Новая наука — термодинамика, — установившая связь между механическими и тепловыми эффектами, обрела существование.
Работа Клаузиуса наглядно показала, что мы не можем неограниченно использовать, казалось бы, неограниченный резервуар энергии, который предоставляет нам природа. Не все процессы, при которых энергия сохраняется, возможны. Например, невозможно создать разность энергий, не уничтожив при этом по крайней мере ее эквивалентность. В идеальном цикле Карно тепло, переносимое от одного источника к другому, есть та цена, которую приходится платить за производимую работу. Осуществив цикл Карно, мы получаем, с одной стороны, произведенную механическую работу, а с другой стороны, перенос тепла, причем то и другое связано между собой отношением эквивалентности. Эта эквивалентность действует в обоих отношениях. Обратным ходом та же машина может восстановить начальную разность температур, затратив произведенную работу. Невозможно построить тепловую машину только с одним источником тепла.
Клаузиуса так же, как и Карно, не интересовали потери, за счет которых кпд всех реальных тепловых машин ниже предсказываемого теорией идеального значения. Теория Клаузиуса так же, как и теория Карно, отвечает некоторой идеализации. Она указывает лишь предел, который устанавливает природа для эффективности тепловых машин.
Но с XVIII в. статус идеализации изменился. Опираясь на закон сохранения энергии, новое естествознание стало претендовать на описание не только идеализаций, но и самой природы, включая «потери». Возникла новая проблема, и в физику вошла необратимость. Как описать то, что происходит в реальной машине? Как включить в баланс энергии потери? Насколько снижают потери кпд реальной машины? Ответы на все эти вопросы проложили путь ко второму началу термодинамики.
4. От технологии к космологии
Как мы уже знаем, вопрос, поднятый Карно и Клаузиусом, привел к теории идеальных тепловых машин, основанной на сохранении энергии и компенсации. Кроме того, стало возможным ставить (и решать) новые проблемы, такие, как диссипация энергии. Уильям Томсон, питавший глубочайшее уважение к работе Фурье, быстро осознал важность этой проблемы и в 1852 г. первым сформулировал второе начало термодинамики.
На теплопроводность, математическую теорию которой построил Фурье, Карно указал как на возможную причину энергетических потерь в тепловом двигателе. Так цикл Карно, уже более не идеальный, а «реальный», стал точкой конвергенции двух универсалий, открытых в XIX в.: превращения энергии и теплопроводности. Сочетание этих двух открытий привело Томсона к формулировке его нового принципа: существования в природе универсальной тенденции к деградации механической энергии. Обращаем особое внимание на слово «универсальная», перекликающееся со словом «универсум», т. е. весь мир, или Вселенная.
Мир Лапласа был идеальным вечным двигателем. Начиная с Томсона, космология перестает быть только отражением нового идеального теплового двигателя, но и включает последствии необратимого распространения тепла в мире, в котором энергия сохраняется. Этот мир космология Томсопа описывала как машину, в которой тепло превращается в движение лишь ценой определенных необратимых потерь и бесполезной диссипации. Соответственно уменьшились различия в природе, способные производить механический эффект. Мир использует эти различия при переходе от одного превращения к другому и стремится к конечному состоянию теплового равновесия — «тепловой смерти». В соответствии с законом Фурье при достижении миром конечного состояния исчезнут всякие различия в температуре, способные производить механический эффект.
Томсон совершил головокружительный прыжок от технологии тепловой машины к космологии. В своей формулировке второго начала термодинамики он использовал научную терминологию середины XIX в.: «сохранение энергии», «тепловой двигатель», «закон Фурье». Немаловажную роль сыграла и культурная среда, в которой было совершено открытие. Общепризнано, что в XIX в. проблема времени приобрела новое значение. Существенную роль времени начали отмечать во всех областях: в геологии, биологии, языкознании, социологии и этике. Вместе с тем интересно отметить, что та специфическая форма, в которой время вошло в физику, именно как тенденция к однородности и смерти, в большей мере напоминает о древних мифологических и религиозных архетипах, чем о все нарастающем усложнении и многообразии, описываемыми биологией и социальными науками. Возвращение этих древних тем можно рассматривать как культурный отзвук социальных и экономических сдвигов времени. Быстрая трансформация технологического способа взаимодействия с природой, постоянно нарастающий темп изменения, с которым столкнулся XIX век, не могли не вызвать тревогу. Это беспокойство не оставляет и нас и принимает самые различные формы в виде повторяющихся призывов к «нулевому росту» общества или к мораторию на научные исследования до провозглашения «научных истин» относительно нашего распадающегося мира. Современные знания в области астрофизики все еще остаются скудными и во многом проблематичными. Трудность продвижения в этой области физики отчасти обусловлена тем, что в астрофизике гравитационные эффекты играют существенную роль и проблемы требуют одновременного использования термодинамики и теории относительности. Тем не менее большинство работ в этой области с удивительным единодушием предсказывает грядущую катастрофу… Одна из последних книг на эту тему рисует такую картину:
«Неприятная истина состоит, по-видимому, в том, что неумолимый распад нашей Вселенной, насколько мы можем судить, неизбежен; организация, охватывающая всякую упорядоченную деятельность от людей до галактик, медленно, но неизбежно деградирует и может даже кануть в небытие в результате всеобщего гравитационного коллапса»14.
Другие более оптимистичны. В превосходной научно-популярной статье об энергии Вселенной Фримен Дайсон пишет следующее:
«Вполне возможно, однако, что жизнь играет более важную роль, чем принято думать. Возможно, что жизни суждено выстоять против всех невзгод, преобразуя мир для собственных целей. И структура неодушевленного мира может оказаться не столь уж далекой от потенциальностей жизни и разума, как имеют обыкновение полагать ученые XX в.»15
Несмотря на существенный прогресс, достигнутый Хокингом и другими исследователями [Наиболее важные результаты были получены Е. М. Лифшицем, Б. Боннором, Дж. Силком, А. Ю. Дж. Пиблсом, Я. Б. Зельдовичем, А. Г. Дорошкевичем, И. Д. Новиковым, Р. А. Сюняевым, С. Ф. Шандариным и др. С современным состоянием теории крупномасштабной структуры Вселенной читатель может познакомиться по следующим работам: сб. Крупномасштабная структура Вселенной. М., 1981; Зельдович Я. Б. Избранные труды. Частицы, ядра Вселенная. М., 1985, особенно с. 280-283.-Прим. перев.], наше знание крупномасштабных преобразований во Вселенной все еще остается неадекватным.
5. Рождение энтропии
В 1865 г. настал черед совершить скачок от технологии к космологии для Клаузиуса. Сначала он лишь переформулировал свои более ранние выводы, но при этом ввел новое понятие — энтропия. Первоначально Клаузиус намеревался четко разграничить понятия сохранения и обратимости. В отличие от механических превращений, для которых обратимость и сохранение совпадают, при физико-химическом превращении энергия может сохраняться даже в том случае, если преобразование необратимо. Это, в частности, относится к трению, когда движение превращается в тепло, или к теплопроводности, описанной Фурье.
Мы уже знакомы с таким понятием, как «энергия». Она является функцией состояния системы, т. е. функцией, зависящей только от значений параметров (давления, объема, температуры) , которые однозначно определяют состояние[16]. Но нам необходимо выйти за рамки закона сохранения энергии и найти способ, позволяющий выразить различие между «полезными» обменами энергией в цикле Карно и «диссипированной» энергией, теряемой необратимо.
Именно такую возможность и предоставляет введенная Клаузиусом новая функция, получившая название «энтропия» и обычно обозначаемая буквой S.
Клаузиус, по-видимому, намеревался лишь записать в новом виде очевидное требование, состоящее в том, что в конце цикла тепловая машина должна возвращаться в начальное состояние. В первом определении энтропии основной акцент делался на сохранении: в конце каждого цикла, идеального или с потерями, функция состояния системы — энтропия — возвращается к своему начальному значению. Но параллель между энтропией и энергией заканчивается, стоит лишь нам отказаться от принятых идеализаций17
Рассмотрим приращение энтропии dS за короткий интервал времени dt. В случае идеальной и реальной тепловой машины ситуация совершенно различная. В первом случае dS можно полностью выразить через теплообмен между машиной и окружающей средой. Можно поставить специальные опыты, в которых система будет отдавать тепло вместо того, чтобы поглощать его. Соответствующее приращение энтропии при этом лишь изменит знак. Такую составляющую полного приращения энтропии мы обозначим deS. Она обратима в том смысле, что может быть и положительной, и отрицательной. В реальных машинах мы сталкиваемся с совершенно иной ситуацией. В них, ломимо обратимого теплообмена, происходят необратимые процессы: тепловые потери, трение и т. д. Они приводят к увеличению энтропии, или производству энтропии, внутри системы. Увеличение энтропии, которое мы обозначим diS, не может изменять знак при обращении теплообмена с внешним миром. Как все необратимые процессы (например, теплопроводность), производство энтропии всегда происходит в одном и том же направлении. Иначе говоря, величина diS может быть только положительной или обращаться в нуль в отсутствие необратимых процессов. Заметим, что положительность diS-вопрос соглашения: с тем же успехом мы могли бы считать величину diS отрицательной. Важно другое: изменение энтропии монотонно; производство энтропии не может изменять знак во времени.
Выбор обозначений deS и diS призван напоминать читателю, что первый член относится к обмену энергией (по-английски exchange — e) с внешним миром, а второй — к необратимым процессам внутри (по английски inside — i) системы. Таким образом, полное приращение энтропии dS представимо в виде суммы двух членов deS и diS, имеющих различный физический смысл18.
Чтобы понять одну специфическую особенность такого разложения приращения энтропии в сумму двух членов, полезно применить наши рассуждения к энергии. Обозначим энергию через Е, и пусть dE — приращение энергии за короткий интервал времени dt. Разумеется, ничто не мешает нам представить dE в виде суммы члена deE, описывающего обмен энергией с внешним миром, и члена diE, связанного с «внутренним производством» энергии. Но закон сохранения энергии утверждает, что энергия никогда не «производится», а лишь переносится с одного места на другое. Следовательно, полное приращение энергии dE сводится к deE. С другой стороны, если мы возьмем какую-нибудь несохраняющуюся величину, например количество молекул водорода в некотором сосуде, то такая величина может изменяться и в результате добавления водорода в сосуд, и вследствие химических реакций, протекающих в сосуде. Знак «производства» несохраняющейся величины заранее не определен. В зависимости от обстоятельств мы можем и производить молекулы водорода, и разрушать их, «отдавая» атомы водорода другим химическим соединениям. Специфическая особенность второго начала состоит в том, что член diS, описывающий производство энтропии, всегда положителен. Производство энтропии отражает необратимые изменения, происходящие внутри системы.
Клаузиусу удалось найти количественное выражение для потока энтропии deS через тепло, поглощаемое (или отдаваемое) системой. В мире, где безраздельно господствуют понятия обратимости и сохранения, вывод такой зависимости имел первостепенное значение. Что же касается необратимых процессов, участвующих в производстве энтропии, то Клаузиус смог установить лишь неравенство diS/dt>0. Но и оно было важным шагом вперед, поскольку позволяло проводить различие между потоком энтропии и производством энтропии не только для цикла Kapно, но и для других термодинамических систем. Для изолированной системы, которая ничем не обменивается с окружающей средой, поток энтропии, по определению, равен нулю. Остается лишь член, описывающий производство энтропии, а энтропия системы может только возрастать или оставаться постоянной. В этом случае сам собой отпадает вопрос о необратимых изменениях, рассматриваемых как приближение к обратимым изменениям: возрастающая энтропия соответствует самопроизвольной, эволюции системы. Энтропия становится, таким образом, «показателем эволюции», или, по меткому выражению Эддингтона, «стрелой времени». Для изолированных систем будущее всегда расположено в направлении возрастания энтропии.
Какая система может быть изолирована лучше, чем наша Вселенная? Эта идея легла в основу космологической формулировки первого и второго начал термодинамики, предложенной Клаузнусом в 1865 г.:
Die Energie der Welt ist konstant.
Die Entropie der Welt strebt einem Maximum zu [19].
[Энергия мира постоянна. Энтропия мира стремится к максимуму (нем.). - Прим. перев.]
Утверждение о том, что энтропия изолированной системы возрастает до максимального значения, выходит за рамки той технологической проблемы, решение которой привело к созданию термодинамики. Возрастающая энтропия перестает быть синонимом потерь. Теперь она относится к естественным процессам внутри системы. Под влиянием этих процессов система переходит в термодинамическое «равновесие», соответствующее состоянию с максимумом энтропии.
В главе 1 мы отмечали элемент некоторой неожиданности в открытии Ньютоном универсальных законов динамики. Когда Сади Карно сформулировал свои законы для идеальных тепловых машин, он не мог даже вообразить, что его работа приведет к концептуальной революции в физике.
Обратимые преобразования принадлежат классической науке в том смысле, что определяют возможность воздействия на систему, управления системой. Динамическим объектом можно управлять, варьируя начальные условия. Аналогичным образом термодинамическим объектом, определяемым в терминах обратимых преобразований, можно управлять, изменяя граничные условия: любая система, находящаяся в состоянии термодинамического равновесия, при постепенном изменении температуры, объема или давления проходит через серию равновесных состояний и при любом обращении производимых над ней манипуляций возвращается в начальное состояние. Обратимый характер таких изменений и управление объектом через граничные условия- процессы взаимозависимые. С этой точки зрения необратимость «отрицательна»: она проявляется в форме неуправляемых изменений, происходящих в тех случаях, когда система выходит из-под контроля. Наоборот, необратимые процессы можно рассматривать как последние остатки самопроизвольной внутренней активности, проявляемой природой, когда человек с помощью экспериментальных устройств пытается обуздать ее.
Таким образом, «отрицательное» свойство — диссипация — показывает, что в отличие от динамических объектов термодинамические объекты управляемы не до конца. Иногда они «выходят из повиновения», претерпевая самопроизвольное изменение.
Для термодинамической системы все изменения не эквивалентны. В этом и состоит физический смысл разложения dS=deS+diS. Самопроизвольное изменение diS, направленное к равновесию, отличается от изменения deS, определяемого и управляемого варьированием граничных условий (например, температуры окружающей среды). В случае изолированной системы равновесие выступает в роли притягивающего множества, или «аттрактора», неравновесных состояний. Следовательно, наше первоначальное утверждение допускает обобщение: эволюция к состоянию-аттрактору отличается от всех других изменений, в особенности от изменений, обусловленных варьированием граничных условий.
Макс Планк часто подчеркивал различие между двумя типами изменений, встречающихся в природе. Природа, писал Планк, по-видимому, отдает «предпочтение» определенным состояниям. Необратимое увеличение энтропии diS/dt описывает приближение системы к состоянию, неодолимо «притягивающему» ее, предпочитаемому ей перед другими, — состоянию, из которого система не выйдет по «доброй воле».
«Согласно этому способу выражения, в природе невозможны те процессы, при которых природа дает меньшее предпочтение конечному состоянию, чем начальному. Предельный случай представляет обратимые процессы; в них природа испытывает одинаковое предпочтение как к начальному, так и к конечному состоянию, и поэтому переход из одного состояния в другое может происходить в обоих направлениях»20.
Сколь чуждым выглядит такой язык по сравнению с языком динамики! В динамике система изменяется вдоль заданной раз и навсегда траектории, не забывая начальную точку (так как начальные условия определяют всю траекторию при любых значениях времени). В случае же изолированной системы все неравновесные ситуации порождают эволюцию к равновесному состоянию одного и того же типа. К моменту достижения равновесия система забывает свои начальные условия, т. е. способ, которым она была приготовлена.
Удельная теплоемкость или сжимаемость системы, находящейся в состоянии термодинамического равновесия, являются свойствами, не зависящими от того, как была построена система. Это счастливое обстоятельство значительно упрощает исследование физических состояний вещества. Действительно, сложные системы состоят из огромного числа частиц*. С точки зрения динамики воспроизвести любое состояние такой системы невозможно из-за бесконечного разнообразия состояний, в которых она может находиться.
Мы сталкиваемся, таким образом, с двумя принципиально различными описаниями: динамикой, применимой к миру движения, и термодинамикой, наукой о сложных системах, наделенных внутренней способностью эволюционировать в сторону увеличения энтропии. Столь резкая противоположность двух описаний немедленно порождает вопрос о том, какая взаимосвязь существует между ними. Эта проблема дискутируется в науке с тех пор, как были сформулированы начала термодинамики.
6. Принцип порядка Больцмана
Второе начало термодинамики содержит два принципиально важных элемента: 1) «негативный», выражающий запрет на некоторые процессы, т. е. их невозможность (тепло может распространяться от горячего источника к холодному, но не от холодильника к нагревателю); 2) «положительный», конструктивный. Второй элемент является следствием первого: запрет на некоторые процессы позволяет нам ввести функцию (энтропию), монотонно возрастающую для изолированных систем. Энтропия ведет себя КАК аттрактор для изолированных систем.
Каким образом положения термодинамики можно было бы совместить с динамикой? В конце XIX в. большинство ученых, по всей видимости, склонны были думать, что термодинамика несовместима с динамикой. Принципы термодинамики были новыми законами, закладывающими фундамент новой науки, не сводимой к традиционной физике. Качественное многообразие энергии и присущую ей тенденцию к диссипации приходилось принимать как новые аксиомы. Таким был аргумент, выдвигаемый «энергетистами» в противовес «атомистам», упорно не желавшим отказаться от выполнения программы, в которой они усматривали высшую миссию физики — сведение сложности явлений природы к простоте поведения элементарных структурных единиц, выражаемого законами движения.
Проблемы перехода от микроскопического уровня к макроскопическому оказались необычайно плодотворными для физики в целом. Первым вызов принял Больцман. Тонкая физическая интуиция подсказывала ему, что необходимо выработать какие-то новые понятия, которые позволили бы обобщить физику траекторий, распространив ее на системы, описываемые термодинамикой. Следуя по стопам Максвелла, Больцман принялся искать концептуальные новации в теории вероятности.
В самой идее о том, что вероятность могла бы играть определенную роль в описании сложных явлений, ничего удивительного не было: у Максвелла она, по-видимому, зародилась под влиянием трудов Кетле, который первым ввел в социологию понятие «среднего» человека. Новацией было введение вероятности в физику не как средства аппроксимации, а как объясняющего принципа, использование ее для демонстрации нового типа поведения систем, состоящих из огромного числа частиц: наличие большой популяции позволяло применять правила теории вероятностей.
Рассмотрим один простой пример применения понятия вероятности в физике. Предположим, что ансамбль из N частиц находится в ящике, разделенном на два равных отделения. Требуется найти вероятность различных распределений частиц между отделениями, т. е. найти вероятность обнаружить N1 частиц в первом отделении (и N2=N-N1 частиц во втором).
Комбинаторный анализ позволяет легко сосчитать число способов, которыми получается каждое из различных распределений N частиц. Например, при N=8 поместить восемь частиц в одну половину ящика можно лишь одним способом. Но если предположить, как это делается в классической физике, что все частицы различимы, то поместить одну частицу в одном отделении, а остальные семь — в другом отделении ящика можно восемью различными способами. Распределить восемь частиц поровну между двумя половинами ящика можно 8!/4!4!=70 различными способами (где n! = 1 2 3… (п-1) n). Аналогичным образом при любом N можно указать число Р способов, которыми можно получить любое заданное распределение (N1, N2), или, как принято говорить в физике, комплексов. Оно определяется выражением P=N!/N1N2!.
Чем больше число комплексов в любом ансамбле частиц, тем меньше отличаются между собой числа N1 и N2. Число комплексов максимально, когда частицы поровну распределены между двумя отделениями ящика. Кроме того, чем больше N, тем больше отличаются между собой числа комплексов, соответствующие различным распределениям. При значениях N порядка 1023, достижимых в макроскопических системах, подавляющее большинство распределений соответствует случаю N1=N2=N/2. Следовательно, для систем, состоящих из большого числа частиц, все состояния, отличающиеся от состояния, которое соответствует равномерному распределению, маловероятны.
Больцман первым понял, что необратимое возрастание энтропии можно было бы рассматривать как проявление все увеличивающегося молекулярного хаоса, постепенного забывания любой начальной асимметрии, поскольку асимметрия приводит к уменьшению числа комплексов по сравнению с состоянием, отвечающим максимальному значению Р. Придя к такому выводу, Больцман решил отождествить энтропию S с числом комплексов: каждое макроскопическое состояние энтропия характеризует числом способов, которым оно может быть достигнуто. Знаменитое соотношение Больцмана S=klnP [Логарифм в этом выражении свидетельствует о том, что энтропия - величина аддитивная (S1+2=S1+S2), тогда как число комплексов Р мультипликативно (P1+2=P1 P2).] выражает ту же идею количественно. Коэффициент пропорциональности k в этой форме — универсальная постоянная, известная под названием «постоянная Больцмана».
Результаты Больцмана означают, что необратимое термодинамическое изменение есть изменение в сторону более вероятных состояний и что состояние-аттрактор есть макроскопическое состояние, соответствующее максимуму вероятности. Такие выводы уводят нас далеко за пределы физики Ньютона. Впервые интерпретация физического понятия была дана в терминах вероятности. Полезность больцмановской интерпретации непосредственно очевидна. Вероятность позволяет адекватно объяснить, почему система забывает любую начальную асимметрию, детали любого конкретного распределения (например, какие частицы были первоначально сосредоточены в данной подобласти системы, или распределение скоростей, возникшее при смешении двух газов с различными температурами). Забывание начальных условий возможно потому, что, как бы ни эволюционировала система, она в конечном счете перейдет в одно из микроскопических состояний, соответствующих макроскопическому состоянию хаоса и максимальной симметрии, поскольку именно такие макроскопические состояния составляют подавляющее большинство всех возможных микроскопических состояний. Коль скоро наиболее вероятное состояние достигнуто, система отклоняется от него лишь на небольшие расстояния и на короткие промежутки времени. Иначе говоря, система лишь флуктуирует около состояния-аттрактора.
Из принципа порядка Больцмапа следует, что наиболее вероятным состоянием, достижимым для системы, является такое, в котором события, происходящие в системе одновременно, статистически взаимно компенсируются. Каково бы ни было начальное распределение в нашем первом примере, эволюция системы в конечном счете приведет к равномерному распределению N1=N2. По достижении этого состояния необратимая макроскопическая эволюция системы завершается. Разумеется, частицы будут по-прежнему переходить из одной половины ящика в другую, но в среднем в любой момент времени число частиц, движущихся в одном направлении, будет совпадать с числом частиц, движущихся в противоположном направлении. В результате движение частиц способно вызывать лишь малые, короткоживущие флуктуации вблизи равновесного состояния N1=N2. Таким образом, вероятностная интерпретация Больцмана позволяет понять специфическую особенность аттрактора, изучаемого равновесной термодинамикой.
На этом история не заканчивается, и всю третью часть нашей книги мы посвятим более подробному обсуждению затронутого круга проблем, а пока ограничимся несколькими замечаниями. В классической (и, как мы увидим в дальнейшем, квантовой) механике все определяется в терминах начальных состояний и законов движения. Каким же образом в описание природы входит вероятность? Обычно, отвечая на этот вопрос, ссылаются на то, что мы не знаем с абсолютной точностью динамическое состояние системы. Это — субъективистская интерпретация энтропии. Такая интерпретация была бы приемлема, если бы необратимые процессы мы рассматривали лишь как досадные помехи, соответствующие трению, или, более общо, как потери при функционировании тепловых машин. Но ныне ситуация изменилась. Как мы увидим, необратимым процессам отводится важнейшая конструктивная роль: так, без них была бы невозможна жизнь. Все это делает субъективистскую интерпретацию весьма спорной. В какой мере допустимо считать, что мы сами являемся результатом неполноты собственного знания, следствием того, что нашему наблюдению доступны лишь макроскопические состояния?
И в термодинамике, и в ее вероятностной интерпретации возникает асимметрия во времени: энтропия возрастает в направлении будущего, но не прошлого. Если мы рассматриваем динамические уравнения, инвариантные относительно обращения времени, то такая асимметрия представляется невозможной. Как мы увидим в дальнейшем, второе начало термодинамики представляет собой принцип отбора, совместимый с динамикой, но не выводимый из нее. Второе начало ограничивает возможные начальные условия, доступные для динамической системы. Следовательно, второе начало термодинамики знаменует радикальный отход от механистического мира классической или квантовой механики. Но вернемся к работам Больцмана.
До сих пор мы рассматривали изолированные системы, в которых число частиц и полная энергия заданы граничными условиями. Но объяснение Больцмана допускает обобщение на открытые системы, взаимодействующие с окружающей средой. В замкнутой системе, определяемой граничными условиями так, что ее температура Т поддерживается постоянной за счет теплообмена с окружающей средой, равновесие соответствует не максимуму энтропии, а минимуму аналогичной функции, получившей название свободной энергии: F=E-TS, где Е — энергия системы, Т — ее температура по так называемой шкале Кельвина (точка замерзания воды соответствует 273 °К, а точка кипения 373 °К).
Соотношение F=E-TS означает, что равновесие есть результат конкуренции между энергией и энтропией, а температура выступает в роли множителя, определяющего относительный вес этих двух факторов. При низких температурах перевес на стороне энергии, и мы наблюдаем образование таких упорядоченных (с малой энтропией) и низкоэнергетических структур, как кристаллы. Каждая молекула внутри таких структур взаимодействует со своими соседями, и их кинетическая энергия мала по сравнению с потенциальной энергией, обусловленной взаимодействиями между соседними молекулами. Каждая молекула как бы скована взаимодействием со своими соседями. При высоких температурах доминирует энтропия и в системе устанавливается молекулярный хаос. Важность относительного движения возрастает, и регулярность в строении кристалла нарушается: по мере увеличения температуры вещество переходит сначала в жидкое, а затем в газообразное состояние.
Энтропия S изолированной системы и свободная энергия системы при заданной температуре являются примерами так называемых термодинамических потенциалов. Экстремумы (т. е. максимумы и минимумы) термодинамических потенциалов, в том числе S и F, задают состояния-аттракторы, к которым самопроизвольно стремится система, если ее граничные условия соответствуют определениям потенциалов.
Принцип порядка Больцмана может быть использован и при исследовании сосуществования структур (например, жидкой и твердой фаз) или равновесия между кристаллизовавшимся продуктом и тем же продуктом в растворе. Не следует, однако, забывать о том, что равновесные структуры определены на молекулярном уровне. Взаимодействие между молекулами на расстоянии порядка 10-8 см, т. е. порядка диаметра атомов в молекулах, делает устойчивой структуру кристаллов и наделяет их макроскопическими свойствами. С другой стороны, размеры кристалла не являются внутренним свойством структуры. Они зависят от того, какое количество вещества находится в кристаллической фазе при равновесии.
7. Карно и Дарвин
Равновесная термодинамика позволяет удовлетворительно объяснить огромное число физико-химических явлений. Тем не менее уместно спросить, охватывает ли понятие равновесной структуры все те различные структуры, с которыми мы сталкиваемся в природе. Ясно, что ответ на подобный вопрос может быть только отрицательным.
Равновесные структуры можно рассматривать как результат статистической компенсации активности микроскопических элементов (молекул, атомов). На глобальном уровне равновесные структуры, по определению, инертны. По той же причине они «бессмертны»: коль скоро равновесная структура образовалась, ее можно изолировать и поддерживать бесконечно долго без дальнейшего взаимодействия с окружающей средой. Но при изучении биологической клетки или города мы сталкиваемся с совершенно другой ситуацией: эти системы не только открыты, но и существуют только потому, что они открыты. Их питают потоки вещества и энергии, которые поступают из внешнего мира. Мы можем изолировать кристалл, но если города и клетки отрезать от окружающей среды, они погибнут. Последние являются неотъемлемой составной частью того мира, из которого они черпают необходимые для себя «питательные вещества», и их невозможно изолировать от потоков, которые они безостановочно перерабатывают.
Но не только живая природа глубоко чужда моделям термодинамического равновесия. Обмен веществом и энергией с окружающей средой происходит также во многих гидродинамических явлениях и в химических реакциях.
Трудно понять, каким образом принцип порядка Больцмана может быть применен во всех таких случаях. То, что с течением времени система становится более однородной, в терминах комплексов интерпретируется вполне естественно: в состоянии однородности, когда забыты «различия», созданные начальными условиями, число комплексов максимально. Но решительно невозможно понять, оставаясь в рамках такого рода представлений, спонтанное возникновение конвекции. Конвективное течение требует когерентности, согласованного поведения огромного числа молекул. Это — противоположность хаоса, привилегированное состояние, которому может соответствовать лишь сравнительно небольшое число комплексов. По терминологии Больцмана, конвективное течение — пример «невероятного» состояния. Но если конвекцию надлежит считать «чудом», то что в таком случае говорить о жизни в ее многочисленных проявлениях и в высшей степеней специфических особенностях даже в случае простейших организмов?
Вопрос о том, в какой мере равновесные модели соответствуют действительности, допускает обращение. Чтобы возникло равновесие, систему необходимо «защитить», «заэкранировать» от потоков, образующих в своей совокупности природу. Система должна быть «запаяна» в консервную банку или помещена в стеклянный сосуд, как гомункулус в гётевском «Фаусте», обращающийся к создавшему его алхимику со следующими словами:
Прижми к груди свое дитя!
Но — бережно, чтоб не разбилась склянка.
Вот неизбежная вещей изнанка:
Природному Вселенная тесна,
Искусственному же замкнутость нужна!
[Гёте И. В. Фауст, часть II. Сцена в лаборатории Вагнера (nepев. Б. Пастернака).]
В привычном нам мире равновесие — состояние редкое и весьма хрупкое. Даже эволюция к состоянию равновесия возможна в мире, очень похожем на наш и находящемся на достаточном удалении от Солнца, чтобы имело смысл говорить по крайней мере о частичной изоляции системы (при температуре Солнца систему вряд ли разумно считать заключенной в «консервную банку»), но в то же время таком, в котором правилом является отсутствие равновесия, «тепличном» мире, где равновесие и неравновесие сосуществуют.
Однако на протяжении довольно длительного периода времени физики считали, что инертная структура кристаллов — единственный предсказуемый и воспроизводимый физический порядок, а приближение к равновесию — единственный тип эволюции, выводимый из фундаментальных законов физики. Любая попытка экстраполяции за пределы термодинамического описания была направлена на то, чтобы определить редкий и непредсказуемый тип эволюции, описанием которого занимаются биология и социальные науки. Как, например, совместить дарвиновскую эволюцию (статистический отбор редких событий) со статистическим исчезновением всех индивидуальных особенностей, всех редких событий, о котором говорит Больцман? Роже Кэллуа поставил вопрос так: «Могут ли и Карно и Дарвин быть правы?»21
Интересно отметить, насколько близок по существу дарвиновский подход к пути, избранному Болъцманом. Вполне возможно, что в данном случае речь идет не просто о внешнем сходстве. Известно, что Больцман с восхищением воспринял идеи Дарвина. По теории Дарвина, сначала происходят спонтанные флуктуации видов, после чего вступает в силу отбор и начинается необратимая биологическая эволюция. Как и у Больцмана, случайность приводит к необратимости. Однако результат эволюции у Дарвина оказывается иным, чем у Больцмана. Интерпретация Больцмана влечет за собой забывание начальных условий, «разрушение» начальных структур, тогда как дарвиновская эволюция ассоциируется с самоорганизацией, с неуклонно возрастающей сложностью.
Резюмируя сказанное, мы можем утверждать, что равновесная термодинамика была первым ответом физики на проблему сложности природы. Этот ответ получил свое выражение в терминах диссипации энергии, забывания начальных условий и эволюции к хаосу. Классической динамике, науке о вечных, обратимых траекториях были чужды проблемы, стоявшие перед XIX в., в которых главная роль отводились понятию эволюции. Равновесная термодинамика оказались в состоянии противопоставить свое представление о времени представлениям других наук: с точки зрения термодинамики время означает деградацию и смерть. Как мы знаем, еще Дидро задавал вопрос: где именно вписываемся в инертный мир, подчиняющийся законам динамики, мы, организованные существа, наделенные способностью воспринимать ощущения? Существует и другой вопрос, над которым человечество билось более ста лет: какое значение имеет эволюция живых существ в мире, описываемом термодинамикой и все более беспорядочном? Какова связь между термодинамическим временем, обращенным к равновесию, и временем, в котором происходит эволюция ко все возрастающей сложности?
Был ли прав Бергсон? Верно ли, что время есть либо само по себе средство инновации, либо вообще ничто?
Глава 5. ТРИ ЭТАПА В РАЗВИТИИ ТЕРМОДИНАМИКИ
1. Поток и сила
Вернемся еще раз к изложению второго начала термодинамики, приведенному в предыдущей главе. Центральную роль в описании эволюции играет понятие энтропии. Как мы уже знаем, приращение энтропии допускает разложение в сумму двух членов: члена deS, связанного с обменом между системой и остальным миром, и члена diS, описывающего производство энтропии вследствие необратимых процессов внутри системы. Второй член всегда положителен, за исключением термодинамического равновесия, когда он обращается в нуль. Для изолированной системы (deS=0) состояние равновесия соответствует состоянию с максимумом энтропии.
Для того чтобы по достоинству оценить значение второго начала для физики, нам понадобится более подробное описание различных необратимых явлений, участвующих в производстве энтропии diS или в производстве энтропии за единицу времени diS/dt.
Особый интерес для нас представляют химические реакции. Вместе с теплопроводностью они являются прототипами необратимых процессов. Помимо того что они важны сами по себе, химические процессы играют первостепенную роль в биологии. В живых клетках идет не прекращающаяся ни на миг метаболическая деятельность. Тысячи химических реакций происходят одновременно для того, чтобы клетка могла получить необходимые питательные вещества, синтезировать специфические биомолекулы и удалить ненужные отходы. Скорости различных реакций так же, как и те места внутри клетки, где они протекают, вся химическая активность клетки строго координированы. Таким образом, биологическая структура сочетает в себе порядок и активность. В отличие от живых структур состояние равновесия остается инертным, даже если оно наделено структурой, как, например, в случае кристалла. Могут ли химические процессы дать нам ключ к постижению различия между поведением кристалла и клетки?
Прежде чем ответить на этот вопрос, нам придется рассмотреть химические реакции с двоякой точки зрения: и с кинетической, и с термодинамической.
С точки зрения кинетики важнейшей величиной является скорость реакции. Классическая теория химической кинетики исходит из допущения, согласно которому скорость химической реакции пропорциональна концентрациям веществ, участвующих в реакции. Действительно, реакция происходит в результате столкновений между молекулами, поэтому совершенно естественно предположить, что число столкновений пропорционально произведению концентраций реагирующих молекул.
Рассмотрим в качестве примера следующую простую реакцию: A+XRB+Y. Такая запись («уравнение реакции») означает, что всякий раз, когда молекула реагента А сталкивается с молекулой реагента X (A и Х — исходные вещества), с определенной вероятностью происходит реакция, в результате которой образуется одна молекула вещества В и одна молекула вещества Y (В и Y — продукты реакции). Столкновение, при котором молекулы подвергаются столь сильной перестройке, называется эффективным. Обычно эффективные столкновения составляют лишь очень малую долю (например, 1/106) от общего числа столкновений. В большинстве случаев молекулы при столкновениях сохраняют свое тождество и лишь обмениваются энергией.
Химическая кинетика занимается изучением изменений концентрации различных веществ, участвующих в реакции. Эти изменения кинетика описывает с помощью дифференциальных уравнений — так же, как механика описывает движение ньютоновскими уравнениями. Но в химической кинетике мы вычисляем не ускорения, а скорости изменения концентраций, и эти скорости представимы в виде некоторых функций от концентраций реагентов. Например, скорость изменения концентрации X [Авторы обозначают концентрации веществ теми же буквами, что и сами вещества. - Прим. перев.],
Т. е. производная dX/dt, пропорциональна произведению концентраций A и X в реакционной смеси, т. е. dX/dt= =-kAX, где k — коэффициент пропорциональности, зависящий от таких величин, как температура и давление, и служащий мерой доли эффективных столкновений, приводящих к реакции A+ХRВ+Y. Поскольку в нашем примере всякий раз, когда исчезает одна молекула вещества X, исчезает также одна молекула вещества А и образуется по одной молекуле веществ В и Y, скорости изменения концентраций реагентов связаны соотношениями: dX/dt = dA/dt = -dY/dt = -dB/dt.
Но если столкновение молекул Х и А может «запустить» химическую реакцию, то столкновение молекул В и Y может привести к обратной реакции. Это означает, что внутри описываемой химической системы может происходить вторая реакция: Y+BRX+A, которая приводит к дополнительному изменению концентрации X: dX/dt=k’YB. Полное изменение концентрации реагента определяется балансом между прямой и обратной реакциями. В нашем примере dX/dt=(-dY/dt=…)=-kAX+ +k’YB.
Будучи предоставленной самой себе, система, в которой происходят химические реакции, стремится к состоянию химического равновесия. Именно поэтому химическое равновесие можно считать типичным примером состояния-аттрактора. Каков бы ни был ее начальный состав, система самопроизвольно достигает этой конечной стадии, в которой прямые и обратные реакции статистически компенсируют друг друга, и поэтому дальнейшее суммарное изменение концентрации любого реагента прекращается (dX/dt=0). В нашем примере из полной компенсации прямой и обратной реакций следует, что равновесные концентрации удовлетворяют соотношению AX/YB=k’/k=K. Оно известно под названием «закона действия масс», или закона Гульдберга-Вааге (К — константа равновесия). Определяемое законом действия масс соотношение концентраций соответствует химическому равновесию так же, как равномерность температуры (в случае изолированной системы) соответствует тепловому равновесию. Соответствующее производство энтропии равно нулю.
Прежде чем перейти к термодинамическому описанию химических реакций, рассмотрим кратко один дополнительный аспект кинетического описания. Скорость химической реакции зависит не только от концентраций реагирующих молекул и термодинамических параметров (например, от давления и температуры). Сказывается на ней и присутствие в системе химических веществ, влияющих на реакцию, но остающихся в итоге неизменными. Такого рода вещества называются катализаторами. Катализаторы могут, например, изменить значения констант реакций k или k’ и даже заставить систему пойти по другому пути реакции. В биологии роль катализаторов играют специфические протеины — ферменты. Эти макромолекулы обладают пространственной конфигурацией, позволяющей им изменять скорость реакции. Ферменты часто бывают высокоспецифичными и влияют лишь на одну реакцию. Возможный механизм каталитического действия ферментов состоит в следующем. В молекуле ферментов имеются места, обладающие повышенной «реакционной способностью». Молекулы других веществ, участвующих в реакции, стремятся присоединиться к активным участкам молекулы фермента. Тем самым повышается вероятность их столкновения, а следовательно, и инициации химической реакции.
Весьма важным типом каталитических процессов (особенно в биологии) являются так называемые автокаталитические реакции, в которых для синтеза некоторого вещества требуется присутствие этого же вещества. Иначе говоря, чтобы получить в результате реакции вещество X, мы должны начать с системы, содержащей Х с самого начала. Например, очень часто молекула Х активирует фермент: присоединяясь к молекуле фермента, Х стабилизирует такую конфигурацию, которая делает легкодоступными активные участки. Автокаталитическим процессам соответствуют схемы реакций типа А+2Х->3Х (в присутствии молекул Х одна молекула А превращается в одну молекулу X). Иначе говоря, нам необходимо иметь X, чтобы произвести еще X. Графически автокаталитическне реакции принято изображать с помощью реакционной петли:
Важная особенность систем с такими реакционными петлями состоит в том, что кинетические уравнения, которые описывают происходящие в них изменения, являются нелинейными дифференциальными уравнениями.
Если мы применим тот же метод, то для реакции A+2XRЗX получим кинетическое уравнение dX/dt=КАХ2, т. е. скорость изменения концентрации вещества Х окажется пропорциональной квадрату его концентрации.
Другой весьма важный класс каталитических реакций в биологии — так называемый кросс-катализ — представлен для системы 2X+YR3X, B+XRY+D на рис. 3.
В данном случае мы действительно имеем дело с кросс-катализом (т. е. «перекрестным катализом»), поскольку из Y получается X, а из Х одновременно получается Y. Катализ не обязательно увеличивает скорость реакции. Он может и замедлять, или ингибировать, ее. Графически это также изображается с помощью соответствующих петель обратной связи.
Характерные математические особенности нелинейных дифференциальных уравнений, описывающих химические реакции с каталитическими стадиями, как мы убедимся в дальнейшем, имеют жизненно важное значение для термодинамики сильно неравновесных химических процессов. Кроме того, как мы уже упоминали, биологами установлено, что петли обратной связи играют весьма существенную роль в метаболических функциях. Например, взаимосвязь между нуклеиновыми кислотами и протеинами может быть описана как кросс-катализ: нуклеиновые кислоты являются носителями информации, необходимой для синтеза протеинов, а протеины в свою очередь синтезируют нуклеиновые кислоты.
Помимо скоростей химических реакций, необходимо также учитывать скорости других необратимых процессов, таких, как перенос тепла и диффузия вещества. Скорости необратимых процессов называются также потоками и обозначаются буквой J. Общей теории, которая давала бы скорости, или потоки, не существует. В химических реакциях скорость зависит от молекулярного механизма, в чем нетрудно убедиться на уже приведенных примерах. Термодинамика необратимых процессов вводит величины еще одного типа: помимо скоростей или потоков J, она использует обобщенные силы X, т. е. «причины», вызывающие потоки. Простейшим примером может служить теплопроводность. Закон Фурье утверждает, что поток тепла J пропорционален градиенту температуры. Следовательно, градиент температуры есть та «сила», которая создает поток тепла. По определению, и поток и силы в состоянии теплового равновесия равны нулю. Как мы увидим в дальнейшем, производство энтропии P=diS/dt может быть вычислено по потоку и силам.
Рассмотрим определение обобщенной силы в случае химической реакции. Для простоты обратимся снова к реакции A+XRY+B. Как мы уже знаем, в случае равновесия соотношение концентраций определяется законом действия масс. Теофил де Донде показал, что в качестве «химической силы» можно ввести сродство A, определяющее направление протекания химической реакции так же, как градиент температуры определяет направление теплового потока. В рассматриваемом нами случае сродство пропорционально lnKBY/AX, где К — константа равновесия. Непосредственно видно, что сродство A обращается в нуль при достижении равновесия, где по закону действия масс AX/BY=K. Если мы станем выводить систему из равновесия, то сродство (по абсолютной величине) возрастет. В этом нетрудно убедиться, если исключить из системы некоторую долю молекул В по мере их образования в ходе реакции. Можно сказать, что сродство служит мерой расстояния между фактическим состоянием системы и ее равновесным состоянием. Кроме того, как мы упоминали, знак сродства определяет направление химической реакции. Если сродство A положительно, то молекул В и Y «слишком много» и суммарная реакция идет в направлении B+YRA+X. И, наоборот, если сродство A отрицательно, то молекул В и Y «слишком мало» и суммарная реакция идет в обратном направлении.
Сродство в том смысле, в каком мы его определили, является уточненным вариантом старинного сродства, о которой писали еще алхимики, стремившиеся разобраться в способности химических веществ вступать в одни и не вступать в другие реакции, т. е. в «симпатиях» и «антипатиях» молекул. Идея о том, что химическая активность не сводима к механическим траекториям, к невозмутимому господству динамических законов, подчеркивалась с самого начала. Мы уже приводили обширную выдержку из Дидро. Позднее Ницше по другому поводу заметил, что смешно говорить о «химических законах», как будто химические вещества подчиняются законам, аналогичным законам морали. В химии, утверждал Ницше, не существует ограничений и каждое вещество вольно поступать как ему «вздумается». Речь идет не об «уважении», питаемом одним веществом к другому, а о силовой борьбе, о непрестанном подчинении слабого сильному2. Химическое равновесие с обращающимся в нуль сродством соответствует разрешению этого конфликта. С этой точки зрения специфичность термодинамического сродства перефразирует на современном языке старую проблему3 — проблему различия между скованным жесткими нормами безразличным миром динамических законов и миром спонтанной продуктивной активности, которому принадлежат химические реакции.
Нельзя не отметить принципиальное концептуальное различие между физикой и химией. В классической физике мы можем по крайней мере представлять себе обратимые процессы, такие, как движение маятника без трения. Пренебрежение необратимыми процессами в динамике всегда соответствует идеализации, но по крайней мере в некоторых случаях эта идеализация разумна. В химии все обстоит совершенно иначе. Процессы, изучением которых она занимается (химические превращения, характеризуемые скоростями реакций), необратимы. По этой причине химию невозможно свести к лежащей в основе классической или квантовой механики идеализации, в которой прошлое и будущее играют эквивалентные роли.
Как и следовало ожидать, все необратимые процессы сопровождаются производством энтропии. Каждый из них входит в diS в виде произведения скорости, или потока J и соответствующей силы X. Полное производство энтропии в единицу времени P=diS/dt равно сумме всех таких вкладов, каждый из которых имеет вид произведения JX.
Термодинамику можно разделить на три большие области, изучение которых соответствует трем последовательным этапам в развитии термодинамики. В равновесной области производство энтропии, потоки и силы равны нулю. В слабо неравновесной области, где термодинамические силы «слабы», потоки Jk линейно зависят от сил. Наконец, третья область называется сильно неравновесной, или нелинейной, потому, что в ней потоки являются, вообще говоря, более сложными функциями сил. Охарактеризуем сначала некоторые общие особенности линейной термодинамики, характерные для слабо неравновесных систем.
2. Линейная термодинамика
В 1931 г. Ларс Онсагер открыл первые общие соотношения неравновесной термодинамики в линейной, слабо неравновесной области. Это были знаменитые «соотношения взаимности». Суть их чисто качественно сводится к следующему: если сила «один» (например, градиент температуры) для слабо неравновесных ситуаций воздействует на поток «два» (например, на диффузию), то сила «два» (градиент концентрации) воздействует на поток «один» (поток тепла). Соотношения взаимности неоднократно подвергались экспериментальной проверке. Например, всякий раз, когда градиент температуры индуцирует диффузию вещества, мы обнаруживаем, что градиент концентрации вызывает поток тепла через систему.
Следует особо подчеркнуть, что соотношения Онсагера носят общий характер. Несущественно, например, происходят ли необратимые процессы в газообразной, жидкой или твердой среде. Соотношения взаимности выполняются независимо от допущений относительно агрегатного состояния вещества.
Соотношения взаимности Онсагера были первым значительным результатом в термодинамике необратимых процессов. Они показали, что предмет этой новой науки не некая плохо определенная «ничейная» земля, а заслуживает внимания ничуть не меньше, чем предмет традиционной равновесной термодинамики, не уступая последнему в плодотворности. Если равновесная термодинамика была достижением XIX в., то неравновесная термодинамика возникла и развивалась в XX в. Вывод соотношений взаимности Онсагера ознаменовал сдвиг интересов от равновесных явлений к неравновесным.
Нельзя не упомянуть и о втором общем результате линейной неравновесной термодинамики. Нам уже приходилось говорить о термодинамических потенциалах, экстремумы которых соответствуют состояниям равновесия, к которому необратимо стремится термодинамическая эволюция. Для изолированной системы потенциалом является энтропия S, для замкнутой системы с заданной температурой — свободная энергия F. Термодинамика слабо неравновесных систем также вводит свой термодинамический потенциал. Весьма интересно, что таким потенциалом является само производство энтропии Р. Действительно, теорема о минимуме производства энтропии утверждает, что в области применимости соотношений Онсагера, т. е. в линейной области, система эволюционирует к стационарному состоянию, характеризуемому минимальным производством энтропии, совместимым с наложенными на систему связями. Эти связи определяются граничными условиями. Например, может возникнуть необходимость поддерживать две точки системы при заданных различных температурах или организовать поток, который бы непрерывно подводил в реакционную зону исходные вещества и удалял продукты реакции.
Стационарное состояние, к которому эволюционирует система, заведомо является неравновесным состоянием, в котором диссипативные процессы происходят с ненулевыми скоростями. Но поскольку это состояние стационарно, все величины, описывающие систему (такие, как температура, концентрации), перестают в нем зависеть от времени. Не зависит от времени в стационарном состоянии и энтропия системы. Но тогда изменение энтропии во времени становится равным нулю: dS=0. Как мы уже знаем, полное приращение энтропии состоит из двух членов: потока энтропии deS и положительного производства энтропии diS; поэтому из равенства dS==0 следует, что deS=-diS<0. Поступающий из окружающей среды поток тепла или вещества определяет отрицательный поток энтропии deS, который компенсируется производством энтропии diS из-за наобратимых процессов внутри системы. Отрицательный поток энтропии deS означает, что система поставляет энтропию внешнему миру. Следовательно, в стационарном состоянии активность системы непрерывно увеличивает энтропию окружающей среды. Все сказанное верно для любых стационарных состояний. Но теорема о минимуме производства энтропии утверждает нечто большее: то выделенное стационарное состояние, к которому стремится система, отличается тем, что в нем перенос энтропии в окружающую среду настолько мал, насколько это позволяют наложенные на систему граничные условия. В этом смысле равновесное состояние соответствует тому частному случаю, когда граничные условия допускают исчезающе малое производство энтропии. Иначе говоря, теорема о минимуме производства энтропии выражает своеобразную «инерцию» системы: когда граничные условия мешают системе перейти в состояние равновесия, она делает лучшее из того, что ей остается, — переходит в состояние энтропии, т. е. в состояние, которое настолько близко к состоянию равновесия, насколько это позволяют обстоятельства.
Таким образом, линейная термодинамика описывает стабильное, предсказуемое поведение систем, стремящихся к минимальному уровню активности, совместимому с питающими их потоками. Из того, что линейная неравновесная термодинамика так же, как и равновесная термодинамика, допускает описание с помощью потенциала, а именно производства энтропии, следует, что и при эволюции к равновесию, и при эволюции к стационарному состоянию система «забывает» начальные условия. Каковы бы ни были начальные условия, система рано или поздно перейдет в состояние, определяемое граничными условиями. В результате реакция такой системы на любое изменение граничных условий становится предсказуемой.
Мы видим, что в линейной области ситуация остается, по существу, такой же, как и в равновесной. Хотя производство энтропии не обращается в нуль, оно тем не менее не мешает необратимому изменению отождествляться с эволюцией к состоянию, полностью выводимому из общих законов. Такое «становление» неизбежно приводит к уничтожению любого различия, любой специфичности. Карно или Дарвин? Парадокс, на который мы обратили внимание в гл. 4, остается в силе. Между появлением естественных организованных форм, с одной стороны, и тенденцией к «забыванию» начальных условий наряду с возникающей при этом дезорганизацией — с другой, все еще существует зияющая брешь.
3. Вдали от равновесия
У истоков нелинейной термодинамики лежит нечто совершенно удивительное, факт, который на первый взгляд легко принять за неудачу: несмотря на все попытки, обобщение теоремы о минимуме производства энтропии для систем, в которых потоки уже не являются более линейными функциями сил, оказалось невозможным. Вдали от равновесия система по-прежнему может эволюционировать к некоторому стационарному состоянию, но это состояние, вообще говоря, уже не определяется с помощью надлежаще выбранного потенциала (аналогичного производству энтропии для слабо неравновесных состояний).
Отсутствие потенциальной функции ставит перед нами вопрос: что можно сказать относительно устойчивости состояний, к которым эволюционирует система? Действительно, до тех пор пока состояние-аттрактор определяется минимумом потенциала (например, производство энтропии), его устойчивость гарантирована. Правда, флуктуация может вывести системы из этого минимума. Но тогда второе начало термодинамики вынудит систему вернуться в исходный минимум. Таким образом, существование термодинамического потенциала делает систему «невосприимчивой» к флуктуациям. Располагая потенциалом, мы описываем «стабильный мир», в котором системы, эволюционируя, переходят в статичное состояние, установленное для них раз и навсегда.
Но когда термодинамические силы, действуя на систему, становятся достаточно «большими» и вынуждают ее покинуть линейную область, гарантировать устойчивость стационарного состояния или его независимость от флуктуации было бы опрометчиво. За пределами линейной области устойчивость уже не является следствием общих законов физики. Необходимо специально изучать, каким образом стационарное состояние реагирует на различные типы флуктуации, создаваемых системой или окружающей средой. В некоторых случаях анализ приводит к выводу, что состояние неустойчиво. В таких состояниях определенные флуктуации вместо того, чтобы затухать, усиливаются и завладевают всей системой, вынуждая ее эволюционировать к новому режиму, который может быть качественно отличным от стационарных состояний, соответствующих минимуму производства энтропии.
Термодинамика позволяет высказать исходное общее заключение относительно систем, в поведении которых могут обнаружиться отклонения от того типа порядка, который диктуется равновесным состоянием. Такие системы должны быть сильно неравновесными. В тех случаях, когда возможна неустойчивость, необходимо указать порог, расстояние от равновесия, за которым флуктуации могут приводить к новому режиму, отличному от «нормального» устойчивого поведения, характерного для равновесных или слабо неравновесных систем.
Чем такой вывод интересен?
Такого рода явления хорошо известны в гидродинамике — теории течений. Например, давно известно, что при определенной скорости ламинарное течение может смениться турбулентным. По свидетельству Мишеля Серра4, древние атомисты уделяли турбулентному течению столь большое внимание, что турбулентность с полным основанием можно считать основным источником вдохновения физики Лукреция. Иногда, писал Лукреций, в самое неопределенное время и в самых неожиданных местах вечное и всеобщее падение атомов испытывает слабое отклонение — «клинамен». Возникающий вихрь дает начало миру, всем вещам в природе. «Клинамен», спонтанное непредсказуемое отклонение, нередко подвергали критике как одно из наиболее уязвимых мест в физике Лукреция, как нечто, введенное ad hoc. В действительности же верно обратное: «клинамен» представляет собой попытку объяснить такие явления, как потеря устойчивости ламинарным течением и его спонтанный переход в турбулентное течение. Современные специалисты по гидродинамике проверяют устойчивость течения жидкости, вводя возмущение, выражающее влияние молекулярного хаоса, который накладывается на среднее течение. Не так уж далеко мы ушли от «клинамена» Лукреция!
Долгое время турбулентность отождествлялась с хаосом или шумом. Сегодня мы знаем, что это не так. Хотя в макроскопическом масштабе турбулентное течение кажется совершенно беспорядочным, или хаотическим, в микроскопическом масштабе оно высокоорганизованно. Множество пространственных и временных масштабов, на которых разыгрывается турбулентность, соответствует когерентному поведению миллионов и миллионов молекул. С этой точки зрения переход от ламинарного течения к турбулентности является процессом самоорганизации. Часть энергии системы, которая в ламинарном течении находилась в тепловом движении молекул, переходит в макроскопическое организованное движение.
Еще одним поразительным примером неустойчивости стационарного состояния, приводящей к явлению спонтанной самоорганизации, может служить так называемая неустойчивость Бенара. Она возникает в горизонтальном слое жидкости с вертикальным градиентом температуры. Нижняя поверхность слоя жидкости нагревается до заданной температуры, более высокой, чем температура верхней поверхности. При таких граничных условиях в слое жидкости устанавливается стационарный поток тепла, идущий снизу вверх. Когда приложенный градиент температуры достигает некоторого порогового значения, состояние покоя жидкости (стационарное состояние, в котором перенос тепла осуществляется только с помощью теплопроводности, без конвекции) становится неустойчивым. Возникает конвекция, соответствующая когерентному, т. е. согласованному, движению ансамблей молекул; при этом перенос тепла увеличивается. Следовательно, при заданных связях (величине градиента температуры) производство энтропии в системе возрастает, что противоречит теореме о минимуме производства энтропии. Неустойчивость Бенара — явление весьма впечатляющее. Конвективное движение жидкости порождает сложную пространственную организацию системы. Миллионы молекул движутся согласованно, образуя конвективные ячейки в форме правильных шестиугольников некоторого характерного размера.
В гл. 4 мы ввели принцип порядка Больцмана, устанавливающий связь энтропии с вероятностью (числом комплексов Р). Применимо ли это соотношение в данном случае? Каждому распределению скоростей молекул соответствует некоторое число комплексов. Оно показывает, сколькими способами мы можем реализовать требуемое распределение скоростей, придавая каждой молекуле некоторую скорость. Все рассуждения аналогичны приведенным в гл. 4 при подсчете числа комплексов как функции от распределения молекул между двумя отделениями ящика. В случае неустойчивости Бенара число комплексов также велико в случае хаоса, т. е. значительного разброса скоростей. Наоборот, когерентное движение означает, что многие молекулы движутся почти с одинаковыми скоростями (разброс скоростей мал). Такому распределению соответствует столь малое число комплексов Р, что вероятность возникновения самоорганизации почти равна пулю. И все же самоорганизация происходит! Мы видим, таким образом, что подсчет числа комплексов, исходящий из гипотезы об априорном равнораспределении вероятностей молекулярных состояний, приводит к неверным выводам. То, что он не соответствует истинному положению вещей, становится особенно заметным, если мы обратимся к происхождению нового режима. В случае неустойчивости Бенара это — флуктуация, микроскопическое конвективное течение, которое, если верить принципу порядка Больцмана, обречено на вырождение, но вопреки ему усиливается и завладевает всей системой. Таким образом, за критическим значением приложенного градиента спонтанно устанавливается новый молекулярный порядок. Он соответствует гигантской флуктуации, стабилизируемой обменом энергией с внешним миром.
В сильно неравновесных условиях понятие вероятности, лежащее в основе больцмановского принципа порядка, становится неприменимым: наблюдаемые структуры не соответствуют максимуму комплексов. Не соответствует максимум комплексов и минимуму свободной энергии F=E-TS. Тенденция к выравниванию и «забыванию» начальных условий перестает быть общей тенденцией. В этом смысле старая проблема происхождения жизни предстает в ином свете. Заведомо ясно, что жизнь несовместима с принципом порядка Больцмана, но не противоречит тому типу поведения, который устанавливается в сильно неравновесных условиях.
Классическая термодинамика приводит к понятию равновесной структуры, примером которой может служить любой кристалл. Ячейки Бенара также представляют собой структуры, но совершенно иной природы. Именно поэтому мы ввели новое понятие — диссипативная структура, чтобы подчеркнуть тесную и на первый взгляд парадоксальную взаимосвязь, существующую в таких ситуациях, с одной стороны, между структурой и порядком, а с другой — между диссипацией, или потерями. В гл. 4 мы видели, что в классической термодинамике тепловой поток считался источником потерь. В ячейке Бенара тепловой поток становится источником порядка.
Таким образом, взаимодействие системы с внешним миром, ее погружение в неравновесные условия может стать исходным пунктом в формировании новых динамических состояний — диссипативных структур. Диссипативная структура отвечает некоторой форме супермолекулярной организации. Хотя параметры, описывающие кристаллические структуры, могут быть выведены из свойств образующих их молекул, и в частности из радиуса действия сил взаимного притяжения и отталкивания, ячейки Бенара, как и все диссипативные структуры, по существу, отражают глобальную ситуацию в порождающей их неравновесной системе. Описывающие их параметры макроскопические — порядка не 10-8см (как расстояния между молекулами в кристалле), а нескольких сантиметров. Временные масштабы также другие: они соответствуют не молекулярным масштабам (например, периодам колебаний отдельных молекул, т. е. порядка 10-15с), а макроскопическим, т. е. секундам, минутам или часам.
Но вернемся к химическим реакциям. Они обладают некоторыми весьма важными отличиями от проблемы Бенара. В ячейке Бенара неустойчивость имеет простое механическое происхождение. Когда мы нагреваем жидкость снизу, нижний слой жидкости становится менее плотным и центр тяжести перемещается вверх. Неудивительно поэтому, что за критической точкой система «опрокидывается» и возникает конвекция.
Химические системы не обладают такого рода механическими свойствами. Можно ли ожидать явления самоорганизации в химических системах? Мысленно мы представляем себе химические реакции так: во всех направлениях в пространстве несутся молекулы веществ и случайным образом сталкиваются. В такой картине не остается места для самоорганизации, и, быть может, в этом заключается одна из причин, по которым химические неустойчивости лишь недавно начали привлекать внимание исследователей. Имеется и еще одно отличие.
 |
Рис. 4. Каталитические петли соответствуют нелинейным членам. В задаче с одной независимой переменной нелинейность означает, что имеется по крайней мере один член, содержащий независимую переменную в степени выше 1. В этом простейшем случае нетрудно проследить за тем, какая связь существует между нелинейными членами и потенциальной неустойчивостью стационарных состояний.
Предположим, что для независимой переменной Х выполняется эволюционное уравнение dX/dt=f(X). Функцию f(X) всегда можно разложить в разность двух функций: f+(X), соответствующую прибыли («наработке» вещества), и f-(X), соответствующую убытку (расходу вещества), каждая из которых положительна или равна 0, т. е. представить в виде f(X)=f+(X)-f-(X). Стационарные состояния dX/dt=0 соответствуют значениям X, при которых f+(X)=f-(X).
Равенство f+(X)=f-(X) означает, что стационарные состояния можно найти, построив точки пересечения графиков функций f+ и f-. Если f+ и f- линейны, то их графики могут пересекаться только в одной точке. В противном случае характер пересечения позволяет сделать выводы об устойчивости соответствующего стационарного состояния.
Возможны следующие четыре случая:
SI. Стационарное состояние устойчиво относительно отрицательных флуктуации и неустойчиво относительно положительных флуктуации. Если систему слегка отклонить влево от SI, то положительная разность между f+ и f- вынудит систему вернуться в SI. Если же систему отклонить вправо от SI, то отклонение будет нарастать.
SS. Стационарное состояние устойчиво как относительно положительных, так и относительно отрицательных флуктуации.
IS. Стационарное состояние устойчиво только относительно положительных флуктуаций.
II. Стационарное состояние неустойчиво как относительно положительных, так и относительно отрицательных флуктуаций.
Все течения достаточно далеко от равновесия становятся турбулентными (порог измеряется в безразмерных числах, например в числах Рейнольдса). Химические реакции ведут себя иначе. Для них большая удаленность от состояния равновесия — условие необходимое, но не достаточное. Во многих химических системах, какие бы связи на них ни накладывались и как бы ни изменялись скорости реакций, стационарное состояние остается устойчивым и произвольные флуктуации затухают, как в слабо неравновесной области. В частности, так обстоит дело в системах, в которых наблюдается цепь последовательных превращений типа A->B->C->D->…, описываемая линейными дифференциальными уравнениями.
Судьба флуктуаций, возмущающих химическую систему, а также новые ситуации, к которым она может эволюционировать, зависят от детального механизма химических реакций. В отличие от систем в слабо неравновесной области поведение сильно неравновесных систем весьма специфично. В сильно неравновесной области не существует универсального закона, из которого можно было бы вывести заключение относительно поведения всех без исключения систем. Каждая сильно неравновесная система требует особого рассмотрения. Каждую систему химических реакций необходимо исследовать особо — поведение ее может быть качественно отличным от поведения других систем.
Тем не менее один общий результат все же был получен, а именно: выведено необходимое условие химической неустойчивости. В цепи химических реакций, происходящих в системе, устойчивости стационарного состояния могут угрожать только стадии, содержащие автокаталитические петли, т. е. такие стадии, в которых продукт реакции участвует в синтезе самого себя. Этот вывод интересен тем, что вплотную подводит нас к фундаментальным достижениям молекулярной биологии (рис. 4).
4. За порогом химической неустойчивости
Изучение химических неустойчивостей в наши дни стало довольно обычным делом. И теоретические, и экспериментальные исследования ведутся во многих институтах и лабораториях. Как мы увидим, эти исследования представляют интерес для широкого круга ученых — не только для математиков, физиков, химиков и биологов, но и для экономистов и социологов.
В сильно неравновесных условиях за порогом химической неустойчивости происходят различные новые явления. Для того чтобы описать их подробно, полезно начать с упрощенной теоретической модели, разработанной в последнее десятилетие в Брюсселе. Американские ученые назвали эту модель «брюсселятором», и это название так и прижилось в научной литературе. (Географические ассоциации, по-видимому, стали правилом в этой области: помимо «брюсселятора», существует «оре-гонатор» и даже самый юный «палоальтонатор»!) Опишем кратко «брюсселятор». Ранее мы уже отмечали те стадии реакции, которые ответственны за неустойчивость (см. рис. 3). Вещество Х образуется из вещества А и превращается в вещество Е. Оно является «партнером» по кросс-катализу вещества Y: Х образуется из Y в результате тримолекулярной стадии, а Y образуется в результате реакции между Х и веществом В.
В этой модели концентрации веществ A, В, D и Е заданы (и являются так называемыми управляющими параметрами). Поведение системы исследуется при возрастающих значениях В. Концентрация А поддерживается постоянной. Стационарное состояние, к которому с наибольшей вероятностью эволюционирует такая система (состояние с dX/dt=dY/dt=0), соответствует концентрациям Х0=А и Y0=B/A. В этом нетрудно убедиться, если выписать кинетические уравнения и найти стационарное состояние. Но как только концентрация В переходит критический порог (при прочих равных параметрах), это стационарное состояние становится неустойчивым. При переходе через критический порог оно становится неустойчивым фокусом, и система, выходя из этого фокуса, выходит, или «наматывается», на предельный цикл. Вместо того чтобы оставаться стационарными, концентрации Х и Y начинают колебаться с отчетливо выраженной периодичностью. Период колебаний зависит от кинетических постоянных, характеризующих скорость реакции, и граничных условий, наложенных на всю систему (температуры, концентрации веществ A, B и т. д.).
За критическим порогом система под действием флуктуаций спонтанно покидает стационарное состояние Х0=A, Y0=В/A. При любых начальных условиях она стремится выйти на предельный цикл, периодическое движение по которому устойчиво. В результате мы получаем периодический химический процесс — химические часы. Остановимся на мгновение, чтобы подчеркнуть, сколь неожиданно такое явление. Предположим, что у нас имеются молекулы двух сортов: «красные» и «синие». Из-за хаотического движения молекул можно было бы ожидать, что в какой-то момент в левой части сосуда окажется больше красных молекул, в следующий момент больше станет синих молекул и т. д. Цвет реакционной смеси с трудом поддается описанию: фиолетовый с беспорядочными переходами в синий и красный. Иную картину мы увидим, разглядывая химические часы: вся реакционная смесь будет иметь синий цвет, затем ее цвет резко изменится на красный, потом снова на синий и т. д. Поскольку смена окраски происходит через правильные интервалы времени, мы имеем дело с когерентным процессом.
Столь высокая упорядоченность, основанная на согласованном поведении миллиардов молекул, кажется неправдоподобной, и, если бы химические часы нельзя было бы наблюдать «во плоти», вряд ли кто-нибудь поверил, что такой процесс возможен. Для того чтобы одновременно изменить свой цвет, молекулы должны «каким-то образом» поддерживать связь между собой. Система должна вести себя как единое целое. К ключевому слову «связь», обозначающему весьма важное для многих областей человеческой деятельности (от химии до нейрофизиологии) понятие, мы будем еще возвращаться неоднократно. Возможно, что именно диссипативные структуры представляют собой один из простейших физических механизмов связи (communication).
Между простейшим механическим осциллятором — пружиной — и химическими часами имеется важное различие. Химические часы обладают вполне определенной периодичностью, соответствующей тому предельному циклу, на который наматывается их траектория. Что же касается пружины, то частота ее колебаний зависит от амплитуды. С этой точки зрения химические часы как хранители времени отличаются большей надежностью, чем пружина.
Но химические часы — отнюдь не единственный тип самоорганизации. До сих пор мы пренебрегали диффузией. В своих рассуждениях мы неизменно предполагали, что все вещества равномерно распределены по всему реакционному пространству. Разумеется, такое допущение не более чем идеализация: небольшие флуктуации всегда создают неоднородности в распределении концентраций и, следовательно, способствуют возникновению диффузии. Следовательно, в уравнениях, описывающих химические реакции, необходимо учитывать диффузию. Уравнения типа «реакция с диффузией» для «брюсселятора» обладают необычайно богатым запасом решений, отвечающих качественно различным типам поведения системы. Если в равновесном и в слабо неравновесном состояниях система остается пространственно однородной, то в сильно неравновесной области появление новых типов неустойчивости, в том числе усиление флуктуаций, нарушает начальную пространственную симметрию. Таким образом, колебания во времени (химические часы) перестают быть единственным типом диссипативных структур, которые могут возникать в системе; в сильно неравновесной области могут появиться, например, колебания не только временные, но и пространственно-временные. Они соответствуют волнам концентраций химических веществ Х и Y, периодически проходящим по системе. Кроме того, в системе, особенно в тех случаях, когда коэффициенты диффузии веществ Х и Y сильно отличаются друг от друга, могут устанавливаться стационарные, не зависящие от времени режимы и возникать устойчивые пространственные структуры.
Здесь нам необходимо еще раз остановиться: на этот раз для того, чтобы подчеркнуть, как сильно спонтанное образование пространственных структур противоречит законам равновесной физики и принципу порядка Больцмана. И в этом случае число комплексов, соответствующих таким структурам, чрезвычайно мало по сравнению с числом комплексов, отвечающих равномерному распределению. Но неравновесные процессы могут приводить к ситуациям, кажущимся немыслимыми с классической точки зрения.
При переходе от одномерных задач к двухмерным или трехмерным число качественно различных диссипативных структур, совместимых с заданным набором граничных условий, возрастает еще больше. Например, в двухмерной области, ограниченной окружностью, может возникнуть пространственно неоднородное стационарное состояние с выделенной осью. Перед нами новый, необычайно интересный процесс нарушения симметрии, особенно если мы вспомним, что одна из первых стадий в морфогенезе зародыша — образование градиента в системе. Такого рода проблемы мы еще рассмотрим и в этой главе, и в гл. 6.
До сих пор мы предполагали, что концентрации А, В, D и Е (наши управляющие параметры) равномерно распределены по всей реакционной системе. Стоит лишь нам отказаться от этого упрощения, как возникают новые явления. Например, система принимает «естественные размеры», зависящие от определяющих параметров. Тем самым система определяет свой внутренний масштаб, т. е. размеры области, занятой пространственными структурами, или часть пространства, в пределах которой проходят периодические волны концентраций.
Все перечисленные выше режимы дают весьма неполную картину необычайного многообразия явлений, возникающих в сильно неравновесной области. Упомянем хотя бы о множественности стационарных состояний. При заданных граничных условиях в сильно нелинейной системе могут существовать не одно, а несколько стационарных состояний, например одно состояние с богатым содержанием вещества X, а другое — с бедным содержанием того же вещества. Переход из одного состояния в другое играет важную роль в механизмах управления, встречающихся в биологических системах.
Начиная с классических работ Ляпунова и Пуанкаре, некоторые характерные точки и линии, а именно фокусы и предельные циклы, известны математикам как аттракторы устойчивых систем. Новым является то, что эти понятия качественной теории дифференциальных уравнений применимы к химическим системам. В этой связи заслуживает быть особо отмеченным тот факт, что первая работа по математической теории неустойчивостей в системе реакций с диффузией была опубликована Тьюрингом в 1952 г. Сравнительно недавно были обнаружены новые типы аттракторов. Они появляются только при большем числе независимых переменных (в «брюсселяторе» число независимых переменных равно двум: это переменные концентрации Х и Y). В частности, в трехмерных системах появляются так называемые странные аттракторы, которым уже не соответствует периодическое движение.
На рис. 8 представлены результаты численных расчетов Хао Байлиня, дающие общее представление об очень сложной структуре такого странного аттрактора для модели, обобщающей «брюсселятор» на случай периодического подвода извне вещества X. Замечательно, что большинство описанных нами типов поведения реально наблюдалось в неорганической химии и в некоторых биологических системах.
В неорганической химии наиболее известным примером колебательной системы является реакция Белоусова-Жаботинского, открытая в начале 50-х гг. нашего века. Соответствующая схема реакций, получившая название орегонатор, была предложена Нойесом и сотрудниками. По существу, она аналогична «брюсселятору», но отличается большей сложностью. Реакция Белоусова-Жаботинского состоит в окислении органической (малоновой) кислоты броматом калия в присутствии соответствующего катализатора — церия, марганца или ферроина.
В различных экспериментальных условиях у одной и той же системы могут наблюдаться различные формы самоорганизации — химические часы, устойчивая пространственная дифференциация или образование волн химической активности на макроскопических расстояниях5.
Обратимся теперь к самому интересному вопросу: что дают все эти результаты для понимания функционирования живых систем?
5. Первое знакомство с молекулярной биологией
Ранее в этой главе мы уже показали, что в сильно неравновесных условиях протекают процессы самоорганизации различных типов. Одни из них приводят к установлению химических колебаний, другие — к появлению пространственных структур. Мы видели, что основным условием возникновения явлений самоорганизации является существование каталитических эффектов.
В то время как в неорганическом мире обратная связь между «следствиями» (конечными продуктами) нелинейных реакций и породившими их «причинами» встречается сравнительно редко, в живых системах обратная связь (как установлено молекулярной биологией), напротив, является скорее правилом, чем исключением. Автокатализ (присутствие вещества Х ускоряет процесс образования его в результате реакции), автоингибиция (присутствие вещества Х блокирует катализ, необходимый для производства X) и кросс-катализ (каждое из двух веществ, принадлежащих различным цепям реакций, является катализатором для синтеза другого) лежат в основе классического механизма регуляции, обеспечивающего согласованность метаболической функции.
Нам бы хотелось подчеркнуть одно любопытное различие. В примерах самоорганизации, известных из неорганической химии, молекулы, участвующие в реакциях, просты, тогда как механизмы реакций сложны (например, в реакции Белоусова-Жаботинского удалось установить около тридцати различных промежуточных соединений). С другой стороны, во многих примерах самоорганизации, известных из биологии, схема реакции проста, тогда как молекулы, участвующие в реакции веществ (протеинов нуклеиновых кислот и т. д.), весьма сложны и специфичны. Отмеченное нами различие вряд ли носит случайный характер. В нем проявляется некий первичный элемент, присущий различию между физикой и биологией. У биологических систем есть прошлое. Образующие их молекулы — итог предшествующей эволюции; они были отобраны для участия в автокаталитических механизмах, призванных породить весьма специфические формы процессов организации.
Описание сложной сети метаболической активности и торможения является существенным шагом в понимании функциональной логики биологических систем. К последней мы относим включение в нужный момент синтеза необходимых веществ и блокирование тех химических реакций, неиспользованные продукты которых могли бы угрожать клетке переполнением.
Основной механизм, с помощью которого молекулярная биология объясняет передачу и переработку генетической информации, по существу, является петлей обратной связи, т. е. нелинейным механизмом. Дезоксирибонуклеиновая кислота (ДНК), содержащая в линейно упорядоченном виде всю информацию, необходимую для синтеза различных основных протеинов (без которых невозможно строительство и функционирование клетки), участвует в последовательности реакций, в ходе которых вся информация кодируется в виде определенной последовательности различных протеинов. Некоторые ферменты осуществляют обратную связь среди синтезированных протеинов, активируя и регулируя не только различные стадии превращений, но и автокаталитический механизм репликации ДНК, позволяющий копировать генетическую информацию с такой же скоростью, с какой размножаются клетки.
Молекулярная биология — один из наиболее ярких примеров конвергенции двух наук. Понимание процессов, происходящих на молекулярном уровне в биологических системах, требует взаимно дополняющего развития физики и биологии, первой — в направлении сложного, второй — простого.
Фактически уже сейчас физика имеет дело с исследованием сложных ситуаций, далеких от идеализации, описываемых равновесной термодинамикой, а молекулярная биология добилась больших успехов в установлении связи живых структур с относительно небольшим числом основных биомолекул. Исследуя множество самых различных химических механизмов, молекулярная биология установила мельчайшие детали цепей метаболических реакций, выяснила тонкую, сложную логику регулирования, ингибирования и активации каталитической функции ферментов, связанных с критическими стадиями каждой из метаболических цепей. Тем самым молекулярная биология установила на микроскопическом уровне основы тех неустойчивостей, которые могут происходить в сильно неравновесных условиях.
В некотором смысле живые системы можно сравнить с хорошо налаженным фабричным производством: с одной стороны, они являются вместилищем многочисленных химических превращений, с другой — демонстрируют великолепную пространственно-временную организацию с весьма неравномерным распределением биохимического материала. Ныне перед нами открывается возможность связать воедино функцию и структуру. Рассмотрим кратко два примера, интенсивно исследовавшиеся в последние годы.
Начнем с гликолиза: цепи метаболических реакций, приводящих к расщеплению глюкозы и синтезу аденозинтрифосфата (АТФ) — универсального аккумулятора энергии, общего для всех живых клеток. При расщеплении каждой молекулы глюкозы две молекулы АДФ (аденозиндифосфата) превращаются в две молекулы АТФ. Гликолиз может служить наглядным примером взаимной дополнительности аналитического подхода биологии и физического исследования устойчивости в сильно неравновесной области6.
В ходе биохимических экспериментов были обнаружены колебания во времени концентраций, связанных с гликолитическим циклом7. Было показано, что эти колебания определяются ключевой стадией в цепи реакций — стадией, активируемой АДФ и ингибируемой АТФ. Это — типично нелинейное явление, хорошо приспособленное к регулированию метаболизма. Всякий раз, когда клетка черпает энергию из своих энергетических резервов, она использует фосфатные связи, и АТФ превращается в АДФ. Таким образом, накопление АДФ внутри клетки свидетельствует об интенсивном потреблении энергии и необходимости пополнить энергетические запасы, в то время как накопление АТФ означает, что расщепление глюкозы может происходить в более медленном темпе.
Теоретическое исследование гликолиза показало, что предложенный механизм действительно может порождать концентрационные колебания, т. е. обеспечивать работу химических часов. Вычисленные из теоретических соображений значения концентраций, необходимые для возникновения колебаний, и величина периода цикла согласуются с экспериментальными данными. Гликолитические колебания вызывают модуляцию всех энергетических процессов в клетке, зависящих от концентрации АТФ, и, следовательно, косвенно влияют на другие метаболические цепи.
Можно пойти еще дальше и показать, что в гликолитическом цикле ход реакций регулируется некоторыми ключевыми ферментами, причем сами реакции протекают в сильно неравновесных условиях. Такие расчеты были выполнены Бенно Хессом8, а полученные результаты обобщены и на другие системы. При обычных условиях; гликолитический цикл соответствует химическим часам, но изменение этих условий может привести к образованию пространственных структур в полном соответствии с предсказаниями на основе существующих теоретических моделей.
С точки зрения термодинамики живая система отличается необычайной сложностью. Одни реакции протекают в слабо неравновесных условиях, другие — в сильно неравновесных условиях. Не все в живой системе «живо». Проходящий через живую систему поток энергии несколько напоминает течение реки — то спокойной и плавной, то низвергающейся водопадом и высвобождающей часть накопленной в ней энергии.
Рассмотрим еще один биологический процесс, также исследованный «на устойчивость»: образование колоний у коллективных амеб Dictyostelium discoideum. Этот процесс9А интересен как пример явления, пограничного между одноклеточной и многоклеточной биологией.
Образование колоний у коллективных амеб — один из наиболее ярких примеров явления самоорганизации в биологической системе, в которой важную роль играют химические часы (см. рис. А).
Выйдя из спор, амебы растут и размножаются как одноклеточные организмы. Так продолжается до тех пор, пока пищи (главным образом, бактерий) достаточно. Как только пищевой ресурс истощается, амебы перестают репродуцироваться и вступают в промежуточную фазу, которая длится около восьми часов. К концу этого периода амебы начинают сползаться к отдельным клеткам, выполняющим функции центров агрегации. Образование многоклеточных колоний, ведущих себя как единый организм, происходит в ответ на хемотаксические сигналы, испускаемые центрами. Сформировавшаяся колония мигрирует до тех пор, пока не обнаружит участок среды с условиями, пригодными для образования плодового тела. Тогда масса клеток начинает дифференцироваться, образуя стебель, несущий на конце мириады спор.
У Dictyostelium. discoideum сползание одноклеточных амеб в многоклеточную колонию происходит не монотонно, а периодически. Как показывает киносъемка процесса образования колоний, существуют концентрические волны амеб, сходящиеся к центру с периодом в несколько минут. Природа хемотаксического фактора известна. Это циклическая АМФ (цАМФ) — вещество, встречающееся во многих биохимических процессах, например в процессах гормональной регуляции. Центры скопления амеб периодически испускают сигналы — порции цАМФ, на которые другие клетки реагируют, перемещаясь к центру и в свою очередь испуская аналогичные сигналы к периферии территории, занимаемой колонией. Существование такого механизма передачи хемотаксических сигналов позволяет каждому центру контролировать колонию, состоящую примерно из 105 амеб.
Как показывает анализ модели образования многоклеточной колонии, существуют два типа бифуркаций: во-первых, агрегация сама по себе представляет нарушение пространственной симметрии; во-вторых, происходит нарушение временной симметрии.
Первоначально амебы распределены равномерно. Когда некоторые из них начинают испускать хемотаксические сигналы, возникают локальные флуктуации в концентрации цАМФ. При достижении критического значения некоторого параметра системы (коэффициента диффузии цАМФ, подвижности амеб и т.д.) флуктуации усиливаются: однородное распределение становится неустойчивым и амебы эволюционируют к неоднородному распределению в пространстве. Это новое распределение соответствует скоплению амеб вокруг центров.
Для того чтобы понять происхождение периодичности в сползании D. discoideum к центрам, необходимо изучить механизм синтеза хемотаксического сигнала. На основе экспериментальных данных этот механизм можно изобразить в виде следующей схемы (рис. В).
На поверхности клетки рецепторы (Р) захватывают молекулы цАМФ. Рецептор обращен во внеклеточную среду и функционально связан с ферментом аденилатциклазой (Ц), преобразующим внутриклеточную АТФ в цАМФ (на рис. цАМФ не обозначена). Синтезированная цАМФ транспортируется через мембрану во внеклеточную среду, где расщепляется фосфодиэстеразой — ферментом, выделяемым амебами. Эксперименты показывают, что захват внемолекулярной цАМФ мембранным рецептором активирует аденилатциклазу (положительная обратная связь обозначена знаком +).
Анализ модели синтеза цАМФ на основе такой автокаталитической регуляции позволил унифицировать различные типы поведения, наблюдаемые при образовании колонии коллективных амеб9В.
Двумя ключевыми параметрами модели являются концентрации аденилатциклазы (s) и фосфодиэстеразы (k). На рис. С, заимствованном из работы Goldbeter A., Segel L.. Differentiation, 1980, 17, p. 127-135, показано поведение модельной системы в пространстве параметров s и k.
В зависимости от значений s и k все пространство этих параметров подразделяется на три области. Область А соответствует устойчивому, невозбудимому стационарному состоянию, область В — устойчивому, но возбудимому стационарному состоянию и область С — режиму незатухающих колебаний вокруг неустойчивого стационарного состояния.
Стрелка указывает возможный «путь развития», соответствующий повышению концентрации фосфодиэстеразы (k) и аденилатциклазы (s), наблюдаемому после начала голодания. Переход из области А в области В и С соответствует наблюдаемым изменениям в поведении: клетки сначала неспособны реагировать на сигналы — внеклеточную цАМФ, затем начинают передавать сигналы дальше и, наконец, обретают способность автономно синтезировать цАМФ в периодическом режиме. Центры колоний являются клетками, для которых параметры k и s быстрее достигают точки внутри области С после начала голодания.
Когда запас питательных веществ в той среде, в которой живут и размножаются коллективные амебы, иссякает, происходит удивительная перестройка (рис. А): отдельные клетки начинают соединяться в колонию, насчитывающую несколько десятков тысяч клеток. Образовавшийся «псевдоплазмодий» претерпевает дифференциацию, причем очертания его непрерывно изменяются. Образуется «ножка», состоящая примерно из трети всех клеток, с избыточным содержанием целлюлозы. Эта «ножка» несет на себе круглую «головку», наполненную спорами, которые отделяются и распространяются. Как только споры приходят в соприкосновение с достаточно питательной средой, они начинают размножаться и образуют новую колонию коллективных амеб. Перед нами наглядный пример приспособления к окружающей среде. Популяция обитает в некоторой области до тех пор, пока не исчерпывает имеющиеся там ресурсы. Затем она претерпевает метаморфозу, в результате которой обретает способность передвигаться и осваивать другие области.
Исследование первой стадии образования колонии показало, что она начинается с волн перемещения отдельных амеб, распространяющихся по их популяции к спонтанно возникающему «центру притяжения». Экспериментальные исследования и анализ теоретических моделей установили, что миграция является откликом клеток на существование в среде градиента концентрации ключевого вещества — циклической АМФ, периодически испускаемого сначала амебой, ставшей центром притяжения, а затем — после срабатывания механизма задержки — и другими амебами. И в этом случае мы видим, какую важную роль играют химические часы. Как уже неоднократно подчеркивалось, они, по существу, являются новым средством связи. В случае коллективных амеб механизм самоорганизации приводит к установлению связи между клетками.
Мы хотели бы подчеркнуть еще один аспект. Образование колоний коллективных амеб — типичный пример того, что можно было бы назвать «порядком через флуктуации»: возникновение «центра притяжения», испускающего циклическую АМФ, сигнализирует о потере устойчивости нормальной питательной среды, т. е. об исчерпании запаса питательных веществ. То, что при нехватке пищевого ресурса любая амеба может начать испускание химических сигналов — циклической АМФ — и, таким образом, стать «центром притяжения» для остальных амеб, соответствует случайному характеру флуктуации. В данном случае флуктуация усиливается и организует среду.
6. Бифуркации и нарушение симметрии
Рассмотрим теперь более подробно, как возникает самоорганизация и какие процессы начинают происходить, когда ее порог оказывается превзойденным. В равновесном или слабо неравновесном состоянии существует только одно стационарное состояние, зависящее от значений управляющих параметров. Обозначим управляющий параметр через ППП (им может быть, например, концентрация вещества В в «брюсселяторе», описание которого приведено в разд. «За порогом химической неустойчивости»). Проследим за тем, как изменяется состояние системы с возрастанием значения В. Увеличивая концентрацию В, мы как бы уводим систему все дальше и дальше от равновесия. При некотором значении В мы достигаем порога устойчивости термодинамической ветви. Обычно это критическое значение называется точкой бифуркации. [На особую роль этих точек обратил внимание Максвелл, размышляя над отношением между детерминизмом и свободой выбора (см. гл. 2 разд. "Язык динамики").]
Рассмотрим некоторые типичные бифуркационные диаграммы. В точке бифуркации В термодинамическая ветвь становится неустойчивой относительно флуктуации (см. рис. 10). При критическом значении lс управляющего параметра l система может находиться в трех различных стационарных состояниях: С, Е и D. Два из них устойчивы, третье неустойчиво. Очень важно подчеркнуть, что поведение таких систем зависит от их предыстории. Начав с малых значений управляющего параметра l и медленно увеличивая их, мы с большой вероятностью опишем траекторию АВС. Наоборот, начав с больших значений концентрации Х и поддерживая постоянным значение управляющего параметра l, мы с высокой вероятностью придем в точку D. Таким образом, конечное состояние зависит от предыстории системы. До сих пор история использовалась при интерпретации биологических и социальных явлений. Совершенно неожиданно выяснилось, что предыстория может играть роль и в простых химических процессах.
Рассмотрим бифуркационную диаграмму, изображенную на рис. 11. От предыдущей диаграммы она отличается тем, что в точке бифуркации появляются два устойчивых решения. В связи с этим, естественно, возникает вопрос: по какому пути пойдет дальнейшее развитие системы после того, как мы достигнем точки бифуркации? У системы имеется «выбор»: она может отдать предпочтение одной из двух возможностей, соответствующих двум неравномерным распределениям концентрации Х в пространстве (рис. 12, 13).
Каждое из этих распределений зеркально симметрично другому: на рис. 12 концентрация Х больше справа, на рис. 13 — слева. Каким образом система выбирает между правым и левым? В этом выборе неизбежно присутствует элемент случайности: макроскопическое уравнение не в состоянии предсказать, по какой траектории пойдет эволюция системы. Не помогает и обращение к микроскопическому описанию. Не существует также различия между правым и левым. Перед нами — случайные явления, аналогичные исходу бросания игральной кости.
Можно было бы ожидать, что при многократном повторении эксперимента при переходе через точку бифуркации система в среднем и половине случаев окажется в состоянии с максимумом концентрации справа, а в половине случаев — в состоянии с максимумом концентрации слева. Возникает другой интересный вопрос. В окружающем нас мире некоторые простые фундаментальные симметрии нарушены[10]. Кто не замечал, например, что большинство раковин закручено преимущественно в одну сторону? Пастер пошел дальше и усмотрел в дисимметрии, т. е. в нарушении симметрии, характерную особенность жизни. Как теперь известно, молекула самой важной нуклеиновой кислоты ДНК имеет форму винтовой линии, закрученной влево. Как возникает такая дисимметрия? Один из распространенных ответов на этот вопрос гласит: дисимметрия обусловлена единичным событием, случайным образом отдавшим предпочтение одному из двух возможных исходов. После того как выбор произведен, в дело вступает автокаталитический процесс и левосторонняя структура порождает новые левосторонние структуры. Другой ответ предполагает «войну» между лево- и правосторонними структурами, в результате которой одни структуры уничтожают другие. Удовлетворительным ответом на этот вопрос мы пока не располагаем. Говорить о единичных событиях вряд ли уместно. Необходимо более «систематическое» объяснение.
Недавно был открыт еще один пример принципиально новых свойств, приобретаемых системами в сильно неравновесных условиях: системы начинают «воспринимать» внешние поля, например гравитационное поле, в результате чего появляется возможность отбора конфигураций.
Каким образом внешнее (например, гравитационное) поле сказалось бы на равновесной ситуации? Ответ на этот вопрос дает принцип порядка Больцмана: все зависит от величины отношения — потенциальная энергия/тепловая энергия. Для гравитационного поля Земли эта величина мала. Чтобы достичь сколько-нибудь заметного изменения давления или химического состава атмосферы, нам понадобилось бы взобраться на достаточно высокую гору. Но вспомним ячейку Бенара. С точки зрения механики ее неустойчивость обусловлена повышением центра тяжести вследствие теплового расширения. Иначе говоря, в эффекте Бенара гравитация играет существенную роль и приводит к новой структуре, несмотря на то что толщина самой ячейки Бенара может достигать лишь нескольких миллиметров. Действие гравитации на столь тонкий слой жидкости было бы пренебрежимо малым в равновесной ситуации, но в неравновесной ситуации, вызванной градиентом температур, приводит даже в таком тонком слое к наблюдаемым макроскопическим эффектам. Неравновесность усиливает действие гравитации11.
В уравнении реакции с диффузией включение гравитации скажется на диффузионном потоке. Как показывают подробные вычисления, влияние гравитации становится особенно ощутимым вблизи точки бифуркации невозмущенной системы. Это позволяет нам, в частности, утверждать, что очень слабые гравитационные поля могут приводить к отбору структур.
Рассмотрим снова систему с бифуркационной диаграммой, изображенной на рис. 11. Предположим, что в отсутствие гравитации, т. е. при g=0, мы имеем, как на рис. 12 и 13, асимметричную конфигурацию «снизу вверх» и ее зеркальное отражение — конфигурацию «сверху вниз». Оба распределения равновероятны, но если включить g, то бифуркационные уравнения изменятся, так как поток диффузии будет содержать член, пропорциональный g. В результате мы получим диаграмму, изображенную на рис. 14. Исходная бифуркационная диаграмма исчезнет, сколь бы малым ни было включенное гравитационное поле. Одна структура а) на новой диаграмме возникает при увеличении параметра бифуркации непрерывно, другая b) достижима лишь при конечном возмущении. Следуя по ветви а), мы ожидаем, что и система будет изменяться непрерывно. Наши ожидания оправдаются при условии, если расстояние S между двумя ветвями велико по сравнению с амплитудой тепловых флуктуации концентрации X. Происходит то, что мы называем «вынужденной» бифуркацией. Как и прежде, вблизи критического значения lс управляющего параметра может произойти самоорганизация. Но теперь одна из двух возможных структур предпочтительнее другой и подлежит отбору.
Важно отметить, что в зависимости от химического процесса, ответственного за бифуркацию, описанный выше механизм может обладать необычайной чувствительностью. Как уже упоминалось, вещество обретает способность воспринимать» различия, неощутимые в равновесных условиях. Столь высокая чувствительность наводит на мысль о простейших организмах, например о бактериях, способных, как известно, реагировать на электрические или магнитные поля. В более общем плане это означает, что в сильно неравновесной химии возможна «адаптация» химических процессов к внешним условиям. Этим сильно неравновесная область разительно отличается от равновесной, где для перехода от одной структуры к другой требуются сильные возмущения или изменения граничных условий.
Еще одним примером спонтанной «адаптивной организации» системы, ее «подстройки» к окружающей среде может служить чувствительность сильно неравновесных состояний к внешним флуктуациям. Приведем один пример12 самоорганизации как функции флуктуирующих внешних условий. Простейшей из всех мыслимых химических реакций является реакция изомеризации АDВ. В нашей модели вещество А может участвовать и в другой реакции: А+светRA*RA+тепло (молекула А, поглощая свет, переходит в возбужденное состояние A*, из которого возвращается в основное состояние, испуская при этом тепло). Мы предполагаем, что обе реакции происходят в замкнутой системе, способной обмениваться с внешним миром только светом и теплом. В системе имеется нелинейность, так как превращение молекулы В в молекулу А сопровождается поглощением тепла: чем выше температура, тем быстрее образуется А. Кроме того, чем выше концентрация А, чем сильнее А поглощает свет и преобразует его в тепло, тем выше температура вещества А. Таким образом, А катализирует образование самого себя.
Можно ожидать, что концентрация А, соответствующая стационарному состоянию, возрастет с увеличением интенсивности света, и действительно так и происходит. Но, начиная с некоторой критической точки, мы сталкиваемся с одним из типичных сильно неравновесных явлений: сосуществованием множественных стационарных состояний. При одних и тех же условиях (например, интенсивности света и температуре) система может находиться в двух различных устойчивых стационарных состояниях, отвечающих двум различным концентрациям А. Третье (неустойчивое) стационарное состояние соответствует порогу между двумя устойчивыми стационарными состояниями. Сосуществование стационарных состояний порождает такое хорошо известное явление, как гистерезис. Но это еще не все. Если интенсивность света вместо того, чтобы быть постоянной, начнет случайным образом флуктуировать, то наблюдаемая нами картина резко изменится. Зона сосуществования двух стационарных состояний расширится, и при некоторых значениях параметров станет возможным сосуществование трех стационарных устойчивых состояний.
В таких положениях случайная флуктуация во внешнем потоке, часто называемая шумом, — отнюдь не досадная помеха: она порождает качественно новые типы режимов, для осуществления которых при детерминистических потоках потребовались бы несравненно более сложные схемы реакций. Важно помнить и о том, что случайный шум неизбежно присутствует в потоках в любой «естественной системе». Например, в биологических или экологических системах параметры, определяющие взаимодействие с окружающей средой, как правило, недопустимо считать постоянными. И клетка, и экологическая ниша черпают все необходимое для себя из окружающей их среды; влага, рН, концентрация солей, свет и концентрация питательных веществ образуют непрестанно флуктуирующую среду. Чувствительность неравновесных состояний не только к флуктуациям, обусловленным их внутренней активностью, но и к флуктуациям, поступающим из окружающей среды, открывает перед биологическими исследованиями новые перспективы.
7. Каскады бифуркаций и переходы к хаосу
В предыдущем разделе мы занимались рассмотрением только первой, или, как предпочитают говорить математики, первичной, бифуркации, которая возникает, когда мы вынуждаем систему перейти порог устойчивости. Далеко не исчерпывая новые решения, которые при этом могут появиться, первичная бифуркация приводит к появлению лишь одного характерного времени (периода предельного цикла) или одной характерной длины. Для того чтобы получить всю картину пространственно-временной активности, наблюдаемой в химических или биологических системах, необходимо продвинуться по бифуркационной диаграмме дальше.
Мы уже упоминали о явлениях, возникающих в результате сложного взаимодействия огромного числа частот в гидродинамических или химических системах. Рассмотрим хотя бы ячейки Бенара, возникающие на определенном расстоянии от равновесия. При дальнейшем удалении от теплового равновесия конвективный поток начинает колебаться во времени. Чем дальше мы уходим от равновесия, тем больше частот появляется в колебаниях, пока наконец не произойдет переход в турбулентный режим13. Взаимодействие колебаний с различными частотами создает предпосылки для возникновения больших флуктуаций. Область на бифуркационной диаграмме, определяемая значениями параметров, при которых возможны сильные флуктуации, обычно принято называть хаотической. Иногда порядок, или когерентность, чередуется с тепловым хаосом и неравновесным турбулентным хаосом. Так происходит, например, в случае неустойчивости Бенара: если увеличивать градиент температуры, то конфигурация конвективных потоков усложнится, появятся колебания, а при дальнейшем увеличение градиента упорядоченная структура исчезнет, уступив место хаосу. Не следует смешивать, однако, равновесный тепловой хаос с неравновесным турбулентным хаосом. В тепловом хаосе, возникающем в равновесных условиях, все характерные пространственные и временные масштабы микроскопического порядка. В турбулентном хаосе число макроскопических пространственных и временных масштабов столь велико, что поведение системы кажется хаотическим. В химии порядок и хаос связаны между собой сложными отношениями: упорядоченные (колебательные) режимы чередуются с хаотическими. Такая перемежаемость, например, наблюдалась в реакции Белоусова-Жаботинского как функция скорости потока.
Во многих случаях довольно трудно провести четкую границу между такими понятиями, как «хаос» и «порядок». К каким системам следует отнести, например, тропический лес: к упорядоченным или хаотическим? История любого вида животных может показаться случайной, зависящей от других видов и флуктуаций окружающей среды. Тем не менее трудно отделаться от впечатления, что общая структура тропического леса, например все многообразие встречающихся в нем видов животных и растений, соответствует некоторому архетипу порядка. Какой бы конкретный смысл мы ни вкладывали в термины «порядок» и «хаос», ясно, что в некоторых случаях последовательность бифуркации приводит к необратимой эволюции и детерминированность характеристических частот порождает все большую случайность, обусловленную огромным числом частот, участвующих в процессе.
Сравнительно недавно внимание ученых привлек необычайно простой путь к хаосу, получивший название последовательность Фейгенбаума. Обнаруженная Фейгенбаумом закономерность относится к любой системе, поведение которой характеризуется весьма общим свойством, а именно: в определенной области значений параметров система действует в периодическом режиме с периодом Т; при переходе через порог период удваивается и становится равным 2Т, при переходе через следующий порог период в очередной раз удваивается и становится равным 4Т и т. д. Таким образом, система характеризуется последовательностью бифуркаций удвоения периода. Последовательность Фейгенбаума — один из типичных маршрутов, ведущих от простого периодического режима к сложному апериодическому, наступающему в пределе при бесконечном удвоении периода. Фейгенбаум открыл, что этот маршрут характеризуется универсальными постоянными, значения которых не зависят от конкретных особенностей механизма, коль скоро система обладает качественным свойством удвоения периода. «Большинство поддающихся измерению свойств любой такой системы в этом апериодическом пределе может быть определено, по существу, без учета каких-либо специфических особенностей уравнения, описывающего каждую конкретную систему…»14
В других случаях (например, в таком, который представлен на рис. 16) эволюция системы содержит как детерминистические, так и стохастические элементы.
На рис. 17 мы видим, что при значении управляющего параметра порядка l6 система может находиться в большом числе устойчивых и неустойчивых режимов. «Историческая» траектория, по которой эволюционирует система при увеличении управляющего параметра, характеризуется чередованием устойчивых областей, где доминируют детерминистические законы, и неустойчивых областей вблизи точек бифуркации, где перед системой открывается возможность выбора одного из нескольких вариантов будущего. И детерминистический характер кинетических уравнений, позволяющих вычислить заранее набор возможных состояний и определить их относительную устойчивость, и случайные флуктуации, «выбирающие» одно из нескольких возможных состояний вблизи точки бифуркации, теснейшим образом взаимосвязаны. Эта смесь необходимости и случайности и составляет «историю» системы.
8. От Евклида к Аристотелю
Одной из наиболее интересных особенностей диссипативных структур является их когерентность. Система ведет себя как единое целое и как если бы она была вместилищем дальнодействующих сил. Несмотря на то что силы молекулярного взаимодействия являются короткодействующими (действуют на расстояниях порядка 10-8 см), система структурируется так, как если бы каждая молекула была «информирована» о состоянии системы в целом.
Утверждение о том, что современная наука родилась тогда, когда на смену пространству Аристотеля (представление о котором было навеяно организацией и согласованностью биологических функций) пришло однородное и изотропное пространство Евклида, высказывалось довольно часто, и мы неоднократно повторяли его. Однако теория диссипативных структур сближает нашу позицию с концепцией Аристотеля. Имеем ли мы дело с химическими часами, концентрационными волнами или неоднородным распределением химических веществ, неустойчивость приводит к нарушению симметрии, как временной, так и пространственной. Например, при движении по предельному циклу никакие два момента времени не являются эквивалентными: химическая реакция обретает фазу, подобно тому как фазой характеризуется световая волна. Другой пример: когда однородное состояние становится неустойчивым и возникает выделенное направление, пространство перестает быть изотропным. Мы движемся, таким образом, от пространства Евклида к пространству Аристотеля!
Трудно удержаться от искушения и не порассуждать о том, что нарушение пространственной и временной симметрии играет важную роль в интереснейших явлениях морфогенеза. Наблюдая эти явления, многие склонялись к выводу, что биологическая система в своем развитии преследует некоторую внутреннюю цель, своего рода план, реализуемый зародышем по мере его роста. В начале XX в. немецкий эмбриолог Ганс Дриш полагал, что развитием зародыша управляет некий нематериальный фактор — энтелехия. Дриш обнаружил, что уже на некоторой ранней стадии зародыш способен выдерживать сильнейшие возмущающие воздействия и, несмотря на них, развиваться в нормальный функционирующий организм. В то же время, просматривая развитие зародыша, отснятое на пленку, мы «видим» скачки, соответствующие качественным реорганизациям тканей, вслед за которыми идут более «спокойные» периоды количественного роста. К счастью, совершаемые при таких скачках ошибки немногочисленны, ибо скачки реализуются воспроизводимо. Мы могли бы считать, что в основе главного механизма эволюции лежит игра бифуркаций как механизмов зондирования и отбора химических взаимодействий, стабилизирующих ту или иную траекторию. Такую идею выдвинул около сорока лет назад биолог Уоддингтон. Для списания стабилизированных путей развития он ввел специальное понятие — креод. По замыслу Уоддингтона, креод должен был соответствовать возможным линиям развития, возникающим под влиянием двойного императива — гиб-кости и надежности15. Ясно, что затронутая Уоддингтоном проблема необычайно сложна, и мы сможем коснуться ее лишь весьма бегло.
Много лет назад эмбриологи ввели понятие морфогенетического поля и высказали гипотезу о том, что дифференциация клетки зависит от ее положения в этом поле. Но как клетка «узнает» о своем положении? Один из возможных ответов состоит в том, что клетка, по-видимому, реагирует на градиент концентрации вещества» определяющего морфогенез, — морфоген. Такие градиенты действительно могли бы возникать в сильно неравновесных условиях из-за неустойчивостей, приводящие к нарушениям симметрии. Если бы возник градиент концентрации морфогена, то каждая клетка оказалась бы в иной окружающей среде, чем остальные, что привело бы к синтезу каждой клеткой своего, специфического набора протеинов. Такая модель, ныне широко используемая, по-видимому, хорошо согласуется с экспериментальными данными. Сошлемся хотя бы на работу Кауфмана по эмбриональному развитию дрозофилы16. В этой работе ответственность за распределение альтернативных программ развития по различным группам клеток в ранней стадии эмбрионального развития возлагается на систему реакций с диффузией. Каждая «секция» зародыша характеризуется единственной комбинацией двоичных выборов, а каждый акт выбора происходит в результате бифуркации, нарушающей пространственную симметрию. Модель Кауфмана позволяет успешно предсказывать исход трансплантации клеток как функции расстояния междy областью, откуда берется пересаживаемая клетка, и областью, куда ее пересаживают, т. е. как функции числа различий между бинарными выборами, или «переключений», определяющих каждый из них.
Такие идеи и модели особенно важны для биологических систем, у которых зародыш начинает развиваться в состоянии, обладающем наружной сферической симметрией (например, бурая водоросль «фукус» или зеленая водоросль «ацетабулярия»). Уместно, однако, спросить: однороден ли зародыш с самого начала? Предположим, что в начальной среде имеются небольшие неоднородности. Являются ли они причиной дальнейшей эволюции или только направляют эволюцию к образованию той или иной структуры? Точные ответы на эти вопросы пока не известны. Но одно установлено определенно: неустойчивость, связанную с химическими реакциями и переносом, можно считать единственным общим механизмом, способным нарушить симметрию первоначально однородного состояния.
Самая возможность такого вывода уводит нас далеко за рамки векового конфликта между редукционистами и антиредукционистами. Со времен Аристотеля неоднократно высказывалось одно и то же убеждение (высказывания Шталя, Гегеля, Бергсона и других антиредукционистов мы уже приводили): чтобы связать между собой различные уровни описания и учесть взаимосвязь между поведением целого и отдельных частей, необходимо понятие сложной организации. В противовес редукционистам, усматривавшим единственную «причину» организации в частях, Аристотель с его формальной причиной, Гегель с его абсолютной идеей в природе, Бергсон с его простым, необоримым актом творения организации утверждали, что целое играет главенствующую роль. Вот что говорится об этом у Бергсона:
«В общем, когда один и тот же объект предстает в одном аспекте как простой, а в другом — как бесконечно сложный, эти два аспекта не равнозначны или, точнее, не обладают реальностью в одной и той же мере. В подобных случаях простота присуща самому объекту, а бесконечная сложность — точкам зрения, с которых объект открывается нам, когда мы, например, обходим вокруг него, символам, в которых наши чувства или разум представляют нам объект, или, более общо, элементам различного порядка, с помощью которых мы пытаемся искусственно имитировать объект, но с которыми он остается несоизмеримым, будучи другой природы, чем они. Гениальный художник изобразил на холсте некую фигуру. Мы можем имитировать его картину многоцветными кусочками мозаики. Контуры и оттенки красок модели мы передадим тем точнее, чем меньше наши кусочки по размеру, чем их больше и чем больше градаций по цвету. Но нам понадобилось бы бесконечно много бесконечно малых элементов с бесконечно тонкой градацией цвета, чтобы получить точный эквивалент фигуры, которую художник мыслил как простую, которую он хотел передать как нечто целое на холсте и которая тем полнее, чем сильнее поражает нас как проекция неделимой интуиции»17.
В биологии конфликт между редукционистами и антиредукционистами часто принимал форму конфликта между утверждением внешней и внутренней целесообразности. Идея имманентного организующего разума тем самым часто противопоставляется модели организации, заимствованной из технологии своего времени (механических, тепловых, кибернетических машин), на что немедленно следует возражение: «А кто построил машину, автомат, подчиняющийся внешней целесообразности?»
Как подчеркивал в начале нашего века Бергсон, и технологическая модель, и виталистская идея о внутренней организующей силе выражают неспособность воспринимать эволюционную организацию без непосредственного ее соотнесения с некоторой предсуществующей целью. И в наши дни, несмотря на впечатляющие успехи молекулярной биологии, концептуальная ситуация остается почти такой же, как в начале XX в.: аргументация Бергсона в полной мере относится к таким метафорам, как «организатор», «регулятор» и «генетическая программа». Неортодоксально мыслящие биологи, такие, как Пол Вейсс и Конрад Уоддингтон18, с полным основанием критиковали такой способ приписывания индивидуальным молекулам способности порождать глобальный биологический порядок, справедливо усматривая в этом негодную попытку разобраться в сути дела, поскольку в действительности решение проблемы ошибочно подменяется ее постановкой.
Вместе с тем нельзя не признать, что технологические аналогии сами по себе представляют определенный интерес для биологии. Но неограниченная применимость таких аналогий означала бы, что между описанием молекулярного взаимодействия и описанием глобального поведения биологической системы, как и в случае, например, электронной цепи, существует принципиальная однородность: функционирование цепи может быть выведено из природы и положения ее узлов; и узлы, и цепь в целом относятся к одному масштабу, поскольку узлы были спроектированы и смонтированы тем же инженером, который разработал и построил всю цепь. В биологии такое, как правило, невозможно.
Правда, когда мы встречаем такую биологическую систему, как бактериальный хемотаксис, бывает трудно удержаться от аналогии с молекулярной машиной, состоящей из рецепторов, сенсорной, регуляторной и двигательной систем. Известно около двадцати или тридцати рецепторов, способных детектировать высокоспецифические классы соединений и заставить бактерию плыть против пространственного градиента аттрактантов (т. е. в сторону повышения концентрации) и по градиенту репеллентов, Такое «поведение» определяется сигналом на выходе системы, обрабатывающей поступающую извне информацию, т. е. положением «тумблера», отвечающего за изменение направления, в котором движется бактерия, в положение «включено» или «выключено»19 .
Но как бы ни поражали наше воображение такие случаи, ими исчерпывается далеко не все. Весьма соблазнительно рассматривать их как предельные случаи, как конечные продукты специфического типа селективном эволюции с акцентом на устойчивости и воспроизводимом поведении в противовес открытости и адаптивности. С этой точки зрения адекватность технологической метафоры — вопрос не принципа, а удобства.
Проблема биологического порядка включает в себя переход от молекулярной активности к надмолекулярному порядку в клетке. Эта проблема далека от своего решения.
Биологический порядок нередко представляют как невероятное физическое состояние, созданное и поддерживаемое ферментами напоминающими демон Максвелла: ферменты поддерживают неоднородность химического состава в системе точно так же, как демон поддерживает разность температур или давлений. Если встать на эту точку зрения, то биология окажется в том положении, которое описывал Шталь. Законы природы разрешают только смерть. Представление Шталя об организующем действии души на этот раз подменяется генетической информацией, содержащейся в нуклеиновых кислотах и проявляющейся в образовании ферментов, которые делают возможным продолжение жизни. Ферменты отодвигают наступление смерти и исчезновение жизни.
Иное значение приобретает (и приводит к иным выводам) биология, если к ней подходить с позиций физики неравновесных процессов. Как теперь известно, и биосфера в целом, и ее различные компоненты, живые или неживые, существуют в сильно неравновесных условиях. В этом смысле жизнь, заведомо укладывающаяся в рамки естественного порядка, предстает перед нами как высшее проявление происходящих в природе процессов самоорганизации.
Мы намереваемся пойти еще дальше и утверждаем, что, коль скоро условия для самоорганизации выполнены, жизнь становится столь же предсказуемой, как неустойчивость Бенара или падение свободно брошенного камня. Весьма примечательно, что недавно были открыты ископаемые формы жизни, обитавшие на Земле примерно в ту эпоху, когда происходило первое горообразование (самые древние из известных ныне ископаемых жили на Земле 3,8?108 лет; возраст Земли считается равным 4,6?109; образование скальных пород также происходило примерно 3,8?109 лет назад). Раннее зарождение жизни, несомненно, является аргументом в пользу идеи о том, что жизнь — результат спонтанной самоорганизации, происходящей при благоприятных условиях. Нельзя не признать, однако, что до количественной теории нам еще очень далеко.
Возвращаясь к нашему пониманию жизни и эволюции, следует заметить, что оно стало существенно более глубоким, и это позволяет нам избежать опасностей, с которыми сопряжена любая попытка полностью опровергнуть редукционизм. Сильно неравновесная система может быть названа организованной не потому, что в ней реализуется план, чуждый активности на элементарном уровне или выходящий за рамки первичных проявлений активности, а по противоположной причине: усиление микроскопической флуктуации, происшедшей в «нужный момент», приводит к преимущественному выбору одного пути реакции из ряда априори одинаково возможных. Следовательно, при определенных условиях роль того или иного индивидуального режима становится решающей. Обобщая, можно утверждать, что поведение «в среднем» не может доминировать над составляющими его элементарными процессами. В сильно неравновесных условиях процессы самоорганизации соответствуют тонкому взаимодействию между случайностью и необходимостью, флуктуациями и детерминистическими законами. Мы считаем, что вблизи бифуркаций основную роль играют флуктуации или случайные элементы, тогда как в интервалах между бифуркациями доминируют детерминистические аспекты. Займемся теперь более подробным изучением этих вопросов.
Глава 6. ПОРЯДОК ЧЕРЕЗ ФЛУКТУАЦИИ
1. Флуктуации и химия
Во введении к книге мы уже говорили о происходящем ныне концептуальном перевооружении физических наук. От детерминистических, обратимых процессов физика движется к стохастическим и необратимым процессам. Это изменение перспективы оказывает сильнейшее влияние на химию. Как мы узнали из гл. 5, химические процессы, в отличие от траекторий классической динамики, соответствуют необратимым процессам. Химические реакции приводят к производству энтропии. Между тем классическая химия продолжает опираться на детерминистическое описание химической эволюции. Как было показано в гл. 5, основным «оружием» теоретиков в химической кинетике являются дифференциальные уравнения, которым удовлетворяют концентрации веществ, участвующих в реакции. Зная эти концентрации в некоторый начальный момент времени (а также соответствующие граничные условия, если речь идет о явлениях, зависящих от пространственных переменных, например о диффузии), мы можем вычислить их в последующие моменты времени. Интересно отметить, что такой детерминистический взгляд на химию перестает соответствовать действительности, стоит лишь перейти к сильно неравновесным процессам.
Мы уже неоднократно подчеркивали роль флуктуаций. Перечислим кратко наиболее характерные особенности их воздействия на систему. Когда система, эволюционируя, достигает точки бифуркации, детерминистическое описание становился непригодным. Флуктуация вынуждает систему выбрать ту ветвь, по которой будет происходить дальнейшая эволюция системы. Переход через бифуркацию — такой же случайный процесс, как бросание монеты. Другим примером может служить химический хаос (см. гл. 5). Достигнув хаоса, мы не можем более прослеживать отдельную траекторию химической системы. Не можем мы и предсказывать детали временного развития. И в этом случае, как и в предыдущем, возможно только статистическое описание. Существование неустойчивости можно рассматривать как результат флуктуации, которая сначала была локализована в малой части системы, а затем распространилась и привела к новому макроскопическому состоянию.
Такая ситуация в корне меняет традиционное представление об отношении между микроскопическим уровнем, описываемым в терминах атомов и молекул, и макроскопическим уровнем, описываемым в терминах таких глобальных переменных, как концентрация. Во многих случаях флуктуации вносят лишь малые поправки. В качестве примера рассмотрим газ, N молекул которого заключены в сосуд объемом V. Разделим этот объем на две равные части. Чему равно число молекул Х в одной из них? Здесь Х — «случайная» переменная, и можно ожидать, что ее значение достаточно близко к N/2.
Основная теорема теории вероятностей (так называемый закон больших чисел) позволяет оценить ошибку, вносимую флуктуациями. По существу, закон больших чисел утверждает, что при измерении X мы можем ожидать значение порядка N/2+ON/2. При большом N ошибка ON/2, вносимая флуктуациями, может быть также большой (например, если N~1024, то ON~1012), но относительная ошибка, вносимая флуктуациями, порядка (ON/2)!(N/2) или 1/ON стремится к нулю при больших N. Как только система становится достаточно большой, закон больших чисел позволяет отличать средние значения от флуктуаций (последние становятся пренебрежимо малыми).
В случае неравновесных процессов встречается прямо противоположная ситуация. Флуктуации определяют глобальный исход эволюции системы. Вместо того чтобы оставаться малыми поправками к средним значениям, флуктуации существенно изменяют средние значения. Ранее такая ситуация нам не встречалась. Желая подчеркнуть ее новизну, мы предлагаем назвать ситуацию, возникающую после воздействия флуктуации на систему, специальным термином — порядком через флуктуацию. Прежде чем приводить примеры порядка через флуктуацию, нам бы хотелось сделать несколько общих замечаний, чтобы подчеркнуть концептуальную новизну той ситуации, с которой мы столкнулись.
Некоторым читателям, должно быть, известны соотношения неопределенности Гейзенберга, выражающие несколько неожиданным образом вероятностный аспект квантовой теории. Возможность одновременного измерения координат и импульса в квантовой теории отпадает, тем самым нарушается и классический детерминизм. Считалось, однако, что это никак не сказывается на описании таких макроскопических объектов, как живые системы. Но роль флуктуаций в сильно неравновесных системах показывает, что это не так. Случайность остается весьма существенной и на макроскопическом уровне. Интересно отметить еще одну аналогию с квантовой механикой, приписывающей волновой характер всем элементарным частицам. Как нам уже известно, сильно неравновесные химические системы также могут обладать когерентным волновым поведением: таковы, например, рассмотренные нами в гл. 5 химические часы. И снова некоторые из особенностей квантовой механики, открытые на микроскопическом уровне, проявляются теперь и на макроскопическом уровне!
Химия активно вовлекается в концептуальное перевооружение физических наук1. По-видимому, мы находимся лишь в самом начале нового направления исследований. Результаты некоторых проведенных в последнее время расчетов наводят на мысль, что в определенных случаях понятие скорости химической реакции может быть заменено статистической теорией, использующей распределение вероятностей реакций2.
2. Флуктуации и корреляции
Вернемся еще раз к химической реакции типа, рассмотренного в гл. 5. Пусть для большей конкретности мы имеем цепь реакций ADXDF. Приведенные в гл. 5 кинетические уравнения относятся к средним концентрациям. Чтобы подчеркнуть это, условимся писать aXn вместо X. Естественно задать вопрос: какова вероятность того, что в данный момент времени концентрация вещества Х имеет то или иное значение? Ясно, что эта вероятность флуктуирует, поскольку флуктуирует число столкновений между молекулами различных веществ, участвующих в реакции. Нетрудно выписать уравнение, описывающее, как изменяется распределение вероятности Р (X, t) в результате процессов рождения и уничтожения молекул X. Для равновесных или стационарных систем это распределение вероятности можно вычислить. Начнем с результатов, которые удается получить для равновесных систем.
В равновесных условиях мы, по существу, открываем заново одно из классических распределений вероятности, известное под названием распределения Пуассона. Оно описано в любом учебнике теории вероятностей, поскольку выполняется в огромном числе самых различных случаев: например, по Пуассону, распределены количество вызовов, поступающих на телефонную станцию, время ожидания в ресторане, флуктуации концентрации частиц в жидкости или газе. Математическая формула, задающая распределение Пуассона, для нас сейчас не имеет значения. Мы хотели бы лишь подчеркнуть два аспекта этого важного распределения. Во-первых, оно приводит к закону больших чисел именно в том виде, в каком он сформулирован в предыдущем разделе; следовательно, в большой системе флуктуации допустимо считать пренебрежимо малыми. Во-вторых, закон больших чисел позволяет нам вычислять корреляции между числом молекул Х в двух точках пространства, находящихся на заданном расстоянии друг от друга. Как показывают вычисления, в равновесных условиях такая корреляция не существует. Вероятность одновременно найти молекулу Х в точке r и молекулу X’ в точке r’ (отличной от точки r) равна произведению вероятности найти молекулу X в точке r и вероятности найти молекулу X’ в точке r’ (мы рассматриваем случай, когда расстояние между точками r и r’ велико по сравнению с радиусом межмолекулярного взаимодействия).
Один из наиболее неожиданных результатов недавних исследований состоял в том, что в неравновесной области ситуация резко изменяется. Во-первых, при подходе вплотную к точкам бифуркации флуктуации становятся аномально сильными и закон больших чисел нарушается. Этого следовало ожидать, так как в сильно неравновесной области система при прохождении точек бифуркации «выбирает» один из различных возможных режимов. Амплитуды флуктуаций имеют такой же порядок величины, как и средние макроскопические значения. Следовательно, различие между флуктуациями и средними значениями стирается. Кроме того, в случае нелинейных химических реакций того типа, который мы рассматривали в гл. 5, появляются дальнодействующие корреляции. Частицы, находящиеся на макроскопических расстояниях друг от друга, перестают быть независимыми. «Отзвуки» локальных событий разносятся по всей системе. Интересно отметить3, что такие дальнодействующне корреляции появляются в самой точке перехода от равновесного состояния к неравновесному. В этом смысле потеря устойчивости равновесным состоянием напоминает фазовый переход, с той лишь особенностью, что амплитуды дальнодействующих корреляций сначала малы, а затем по мере удаления от равновесного состояния нарастают и в точках бифуркаций могут обращаться в бесконечность.
Мы считаем, что такой тип поведения представляет особый интерес, поскольку позволяет подвести «молекулярную основу» под обсуждавшуюся ранее при рассмотрении химических часов проблему связи между частицами. Дальнодействующие корреляции организуют систему еще до того, как происходит макроскопическая бифуркация. Мы снова возвращаемся к одной из главных идей нашей книги: к неравновесности как источнику порядка. В данном случае ситуация особенно ясна. В равновесном состоянии молекулы ведут себя независимо: каждая из них игнорирует остальные. Такие независимые частицы можно было бы назвать гипнонами («сомнамбулами»). Каждая из них может быть сколь угодно сложной, но при этом «не замечать» присутствия остальных молекул. Переход в неравновесное состояние пробуждает гипноны и устанавливает когерентность, совершенно чуждую их поведению в равновесных условиях. Аналогичную картину рисует и микроскопическая теория неравновесных процессов, с которой мы познакомимся в гл.9.
Активность материи связана с неравновесными условиями, порождаемыми самой материей. Так же как и в макроскопическом поведении, законы флуктуации и корреляций в равновесных условиях (когда мы обнаруживаем распределение Пуассона) носят универсальный характер. При переходе границы, отделяющей равновесную область от неравновесной, они утрачивают универсальность и обретают сильнейшую зависимость от типа нелинейности системы.
3. Усиление флуктуаций
Рассмотрим сначала два примера, на которых во всех подробностях можно проследить за ростом флуктуаций, предшествующим образованию новой структуры. Первый пример — образование колонии коллективных амеб, стягивающихся при угрозе голода в единую многоклеточную массу. В гл. 5 мы уже упоминали об этом ярком примере самоорганизации. Другой иллюстрацией роли флуктуации может служить первая стадия постройки гнезда термитами. Она была впервые описана Грассе, а Денюбург исследовал ее с интересующей нас точки зрения4.
Процесс самоорганизации в популяции насекомых
Личинки жука Dendroctonus micans [Scol.] первоначально случайным образом распределены между двумя горизонтальными стеклянными пластинками с зазором 2 мм. С боковых сторон пространство между пластинками открыто. Площадь поверхности 400 см2.
Скопление личинок происходит под влиянием конкуренции двух факторов: случайных движений личинок и их реакции на особое химическое вещество феромон, синтезируемое личинками из терпенов, содержащихся в дереве, которым они питаются. Личинки испускают феромоновые сигналы с частотой, зависящей от степени насыщения. Феромон диффундирует в пространстве, и личинки перемещаются в направлении, задаваемом градиентом его концентрации. Такая реакция является автокаталитическим механизмом, поскольку скопление личинок увеличивает притягательность соответствующей области. Чем выше локальная плотность личинок в данной области, тем выше градиент концентрации феромона и тем сильнее тенденция других личинок к сползанию в точку скопления.
Как показывает эксперимент, плотность популяцни личинок определяет не только скорость, но и эффективность процесса самоорганизации, т.е. число личинок в скоплении на его конечном этапе. При большой плотности (рис. А) скопление возникает и быстро растет в центре экспериментальной установки. При очень малых плотностях устойчивое скопление не образуется (рис. В).
В других экспериментах исследовалась возможность образования, скопления личинок из «ядра», искусственно созданного на периферии системы. В зависимости от числа личинок в начальном ядре возникают различные ситуации (рис. С).
Если число личинок в ядре мало по сравнению с общим числом личинок, то скопление не образовывалось (рис. D) Если же число. личинок в ядре велико, то скопление растет (рис. Е). При среднем (не слишком большом и не слишком малом) числе личинок в ядре могут возникать структуры новых типов: появляются и сосуществуют два, три или четыре новых скопления с временем жизни не меньшим, чем время наблюдения (рис. F и G).
В экспериментах с однородными начальными условиями такие многокластерные структуры никогда не наблюдались. По-видимому, на бифуркационной диаграмме они соответствуют устойчивым состояниям при допустимых значениях параметров, характеризующих систему, недостижимых из однородных начальных условий. Затравочное ядро выполняет функцию своего рода возмущения, которым необходимо воздействовать на систему для того, чтобы возбудить ее и перевести в область бифуркационной диаграммы, соответствующей» семействам многокластерных распределений.
Постройка гнезда (термитника) термитами — одна из тех когерентных активностей, которые дали некоторым ученым повод для умозрительных утверждений о «коллективном разуме» в сообществах насекомых. Проявляется этот «коллективный разум» довольно необычным способом: для участия в постройке такого огромного и сложного сооружения, как термитник, термитам необходимо очень мало информации. Первая стадия строительной активности (закладка основания), как показал Грассе, является результатом внешне беспорядочного поведения термитов. На этой стадии они приносят и беспорядочно разбрасывают комочки земли, но каждый комочек пропитывают гормоном, привлекающим других термитов. Ситуацию можно представить следующим образом: начальной «флуктуацией» является несколько большая концентрация комочков земли, которая рано или поздно возникнет в какой-то точке области обитания термитов. Возросшая плотность термитов в окрестности этой точки, привлеченных несколько большей концентрацией гормона, приводит к нарастанию флуктуации. Поскольку число термитов в окрестности точки увеличивается, постольку вероятность сбрасывания ими комочков земли в этой окрестности возрастает, что в свою очередь приводит к увеличению концентрации гормона-аттрактанта. Так воздвигаются «опоры». Расстояние между ними определяется радиусом распространения гормона. Недавно были описаны и другие аналогичные примеры.
Хотя принцип порядка Больцмана позволяет описывать химические или биологические процессы, в которых неоднородности выравниваются, а начальные условия забываются, он не может объяснить ситуации, подобные только что описанным, где несколько «решений», принятых в условиях потери устойчивости, могут направить развитие системы, состоящей из большого числа взаимодействующих единиц, к некоторой глобальной структуре.
Когда новая структура возникает в результате конечного возмущения, флуктуация, приводящая к смене режимов, не может сразу «одолеть» начальное состояние. Она должна сначала установиться в некоторой конечной области и лишь затем распространиться и «заполнить» все пространство. Иначе говоря, существует механизм нуклеации. В зависимости от того, лежат ли размеры начальной области флуктуации ниже или выше критического значения (в случае химических диссипативных структур этот порог зависит, в частности, от кинетических констант и коэффициента диффузии), флуктуация либо затухает, либо распространяется на всю систему. Явления нуклеации хорошо известны из классической теории фазового перехода: например, в газе непрестанно образуются и затем испаряются капельки конденсата. Когда же температура и давление достигают точки, в которой становится устойчивым жидкое состояние, может образоваться капля критических размеров (тем меньших, чем ниже температура и чем выше давление), Если размеры капли превышают порог нуклеации, газ почти мгновенно превращается в жидкость.
Как показывают теоретические исследования и численное моделирование, критические размеры ядра возрастают с эффективностью механизмов диффузии, связывающих между собой все области системы. Иначе говоря, чем быстрее передается сигнал по «каналам связи» внутри системы, тем выше процент безрезультатных флуктуаций и, следовательно, тем устойчивее система. Этот аспект проблемы критического размера означает, что в подобных ситуациях «внешний мир», т. е. все, что окружает флуктуирующую область, всегда стремится погасить флуктуации. Затухнут ли флуктуации или усилятся, зависит от эффективности «канала связи» между флуктуирующей областью и внешним миром. Таким образом, критические размеры определяются конкуренцией между «интегративной силой» системы и химическими механизмами, приводящими к усилению флуктуации.
Описанная нами модель применима, в частности, к результатам, полученным в последнее время in vitro при экспериментальных исследованиях зарождения раковых опухолей5. В этих исследованиях отдельная раковая клетка рассматривается как флуктуация, способная спонтанно и непрестанно появляться и размножаться посредством репликации. Возникнув, раковая клетка сталкивается с популяцией цитотоксических клеток и либо погибает, либо выживает. В зависимости от значений различных параметров, характеризующих процессы репликации и гибели раковых клеток, мы можем предсказывать либо регресс, либо разрастание опухоли. Такого рода кинетические исследования привели к открытию неожиданных свойств взаимодействия цитотоксических клеток и опухоли: было установлено, что цитотоксические клетки могут принимать мертвые опухолевые клетки за живые. Такие ошибки существенно затрудняют разрушение опухоли.
Вопрос о пределах сложности системы поднимался довольно часто. Действительно, чем сложнее система, тем более многочисленны типы флуктуаций, угрожающих ее устойчивости. Позволительно, однако, спросить, как же в таком случае существуют такие сложные системы, какими является экологическая или социальная структура человеческого общества? Каким образом им удается избежать перманентного хаоса? Частичным ответом на подобные вопросы может быть ссылка на стабилизирующее влияние связи между частями систем, процессов диффузии. В сложных системах, где отдельные виды растений, животных и индивиды вступают между собой в многочисленные и разнообразные взаимодействия, связь между различными частями системы не может не быть достаточно эффективной. Между устойчивостью, обеспечиваемой связью, и неустойчивостью из-за флуктуации имеется конкуренция. От исхода этой конкуренции зависит порог устойчивости.
4. Структурная устойчивость
В каких случаях мы начинаем говорить об эволюции в ее собственном смысле? Как известно, диссипативные структуры требуют сильно неравновесных условий. Тем не менее уравнения реакций с диффузией содержат параметры, допускающие сдвиг в слабо неравновесную область. На бифуркационной диаграмме система может эволюционировать и приближаясь к равновесию, и удаляясь от него, подобно тому как жидкость может переходить от ламинарного течения к турбулентному и возвращаться к ламинарному. Сколько-нибудь жесткой и определенной схемы эволюции не существует.
С совершенно иной ситуацией мы встречаемся в моделях, в которых размеры системы входят в качестве параметра бифуркации: рост, происходящий необратимо во времени, приводит к необратимой эволюции. Однако такой тип развития является достаточно узким частным случаем, хотя вполне возможно, что он имеет некоторое отношение к морфогенетическому развитию.
Ни в биологической, ни в экологической или социальной эволюции мы не можем считать заданным определенное множество взаимодействующих единиц или определенное множество преобразований этих единиц. Это означает, что определение системы необходимо модифицировать в ходе эволюции. Простейший из примеров такого рода эволюции связан с понятием структурной устойчивости. Речь идет о реакции заданной системы на введение новых единиц, способных размножаться и вовлекать во взаимодействие различные процессы, протекающие в системе.
Проблема устойчивости системы относительно изменений такого типа сводится к следующему. Вводимые в небольшом количестве в систему новые составляющие приводят к возникновению новой сети реакций между ее компонентами. Новая сеть реакций начинает конкурировать со старым способом функционирования системы. Если система структурно устойчива относительно вторжения новых единиц, то новый режим функционирования не устанавливается, а сами новые единицы («инноваторы») погибают. Но если структурные флуктуации успешно «приживаются» (например, если новые единицы размножаются достаточно быстро и успевают «захватить» систему до того, как погибнут), то вся система перестраивается на новый режим функционирования: ее активность подчиняется новому «синтаксису»6.
Простейшим примером такого рода может служить популяция макромолекул, образующихся в результате-полимеризации внутри системы, в которую поступают мономеры А и В. Предположим, что процесс полимеризации автокаталитический, т. е. синтезированный полимер используется в качестве образца для образования цепи с той же последовательностью структурных единиц. Такого рода синтез протекает гораздо быстрее, чем синтез в отсутствие образца для копирования. Каждый тип полимеров, отличающийся от других последовательностью расположения в цепи молекул А и В, может быть описан набором параметров, задающих скорость катализируемого синтеза копии, точность процесса копирования и среднее время жизни самой макромолекулы. Можно показать, что при определенных условиях в популяции доминирует полимер какого-то одного типа, например АВАВАВА…, а остальные полимеры могут рассматриваться как «флуктуации» относительно него. Возникающая всякий раз проблема структурной устойчивости обусловлена тем, что в результате «ошибки» при’ копировании эталонного образца в системе возникает полимер нового типа, характеризуемый ранее не встречавшейся последовательностью мономеров А и В и новым набором параметров, который начинает размножаться, конкурируя с доминантными видам и за обладание мономерами А и В. Перед нами простейший вариант классической дарвиновской идеи о «выживании наиболее приспособленного».
Аналогичные идеи положены в основу модели предбиотической эволюции, разработанной Эйгеном и его сотрудниками. Подробности теории Эйгена можно найти в многочисленных статьях и книжных публикациях7, поэтому мы ограничимся лишь изложением самой сути. Эйген и его сотрудники показали, что только система одного типа обладает способностью сопротивляться «ошибкам», постоянно совершаемым автокаталитическими популяциями, — а именно полимерная система, структурно устойчивая относительно появления любого полимера-»мутанта». Такая система состоит из двух множеств полимерных молекул. Молекулы первого множества выполняют функцию «нуклеиновых кислот». Каждая молекула обладает способностью к самовоспроизведению и действует как катализатор при синтезе молекул второго множества, выполняющих функцию «протеинов». Каждая молекула второго множества катализирует самовоспроизведение молекул первого множества. Такая кросс-каталитическая связь между молекулами двух множеств может превращаться в цикл (каждая «нуклеиновая кислота» воспроизводит себя с помощью «протеина»). Этот цикл обеспечивает устойчивое выживание «нуклеиновых кислот» и «протеинов», защищенных от постоянно возникающих с высоким коэффициентом воспроизводства новых полимеров: ничто не может вмешиваться в самовоспроизводящийся цикл, образуемый «нуклеиновыми кислотами» и «протеинами». Таким образом, эволюция нового типа начинает расти на прочном фундаменте, предвосхищающем появление генетического кода.
Подход, предложенный Эйгеном, несомненно, представляет большой интерес. В среде с ограниченным запасом питательных веществ дарвиновский отбор имеет важное значение для точного самовоспроизведения. Но нам хотелось бы думать, что это не единственный аспект предбиотической эволюции. Не менее важное значение имеют сильно неравновесные условия, связанные с критическими, пороговыми значениями потоков энергии и вещества. По-видимому, разумно предположить, что некоторые из первых стадий эволюции к жизни были связаны с возникновением механизмов, способных поглощать и трансформировать химическую энергию, как бы выталкивая систему в сильно неравновесные условия. На этой стадии жизнь, или «преджизнь», была редким событием и дарвиновский отбор не играл такой существенной роли, как на более поздних стадиях.
В нашей книге отношению между микроскопическим и макроскопическим уделяется немало внимания. Одной из наиболее важных проблем в эволюционной теории является возникающая в итоге обратная связь между макроскопическими структурами и микроскопическими событиями: макроскопические структуры, возникая из микроскопических событий, должны были бы в свою очередь приводить к изменениям в микроскопических механизмах. Как ни странно, но в настоящее время наиболее понятные случаи относятся к ситуациям, возникающим в человеческом обществе. Когда мы прокладываем дорогу или строим мост, мы можем предсказать, как это скажется на поведении окрестного населения, а оно в свою очередь определяет изменения в характере и способах связи внутри региона. Такие взаимосвязанные процессы порождают очень сложные ситуации, и это обстоятельство необходимо сознавать, приступая к их моделированию. Именно поэтому мы ограничимся описанием лишь четырех наиболее простых случаев.
5. Логистическая эволюция
Понятие структурной устойчивости находит широкое применение в социальных проблемах. Следует, однако, подчеркнуть, что всякий раз речь идет о сильном упрощении реальной ситуации, описываемой в терминах конкуренции между процессами саморепликации в среде с ограниченными пищевыми ресурсами.
В экологии классическое уравнение, описывающее такую проблему, называется логистическим уравнением. Оно описывает, как эволюционирует популяция из N особей с учетом рождаемости, смертности и количества ресурсов, доступных популяции. Логистическое уравнение можно представить в виде dN/dt=rN(K-N)-mN, где r и m — характерные постоянные рождаемости и смертности, К — «несущая способность» окружающей среды. При любом начальном значении N система со временем выходит на стационарное значение N=K-m/r, зависящее от разности между несущей способностью среды и отношением постоянных смертности и рождаемости. При достижении этого стационарного значения наступает насыщение: в каждый момент времени рождается столько индивидов, сколько их погибает.
Кажущаяся простота логистического уравнения до некоторой степени скрывает сложность механизмов, участвующих в процессе. Мы уже упоминали о внешнем шуме. В случае логистического уравнения он имеет особенно простой смысл. Ясно, что при учете одних лишь климатических флуктуаций коэффициенты К, т и r нельзя считать постоянными: как хорошо известно, такие флуктуации могут разрушить экологическое равновесие и даже обречь популяцию на полное вымирание. Разумеется, в системе начинаются новые процессы, такие, как создание запасов пищи и образование новых колоний, которые заходят в своем развитии настолько далеко, что позволяют в какой-то мере избежать воздействия внешних флуктуации.
Есть в логистической модели и другие тонкости. Вместо того чтобы записывать логистическое уравнение в непрерывном времени, будем сравнивать состояние популяции через заданные интервалы времени (с интервалом, например, в год). Такое дискретное логистическое уравнение представимо в виде Nt+1=Nt(l+r[1-Nt/K]), где Nt и Nt+1 — популяции с интервалом в один год (членом, учитывающим смертность, мы пренебрегаем). Р. Мэй8 обратил внимание на одну замечательную особенность таких уравнений: несмотря на их простоту, они допускают необычайно много решений. При значениях параметра 0?r?2 в дискретном случае так же, как и в непрерывном, наблюдается монотонное приближение к равновесию. При значениях параметра 2До сих пор мы рассматривали все со статической точки зрения. Обратимся теперь к механизмам, позволяющим варьировать параметры К, r и m в ходе биологической или экологической эволюции.
Следует ожидать, что в процессе эволюции значения экологических параметров К, r и m будут изменяться (так же как и многих других параметров и переменных независимо от того, допускают ли они квантификацию или не допускают). Живые сообщества непрестанно изыскивают новые способы эксплуатации существующих ресурсов или открытия новых (увеличивая тем самым значение параметра К), продления жизни или более быстрого размножения. Каждое экологическое равновесие, определяемое логистическим уравнением, носит лишь временный характер, и логистически заданная экологическая ниша последовательно заполняется серией видов, каждый из которых вытесняет предшествующие, когда его «способность» к использованию ниши, измеряемая величиной К-m/r, становится больше, чем у них (см. рис. 21). Таким образом, логистическое уравнение описывает весьма простую ситуацию, позволяющую количественно сформулировать дарвиновскую идею о выживании «наиболее приспособленного»: наиболее приспособленным считается тот вид, у которого в данный момент времени величина К-т/r больше.
Сколь ни ограниченна задача, описываемая логистическим уравнением, однако и она приводит к некоторым поистине замечательным примерам изобретательности природы.
Возьмем хотя бы гусениц, которые должны оставаться незамеченными, поскольку они движутся слишком медленно, чтобы успеть скрыться от врага.
Выработанные в процессе эволюции стратегии, включающие использование ядов, едких веществ, раздражающих волосков и игл, оказываются высокоэффективными при отпугивании птиц и других потенциальных хищников. Но ни одна из этих стратегий не обладает универсальной эффективностью, способной надежно защитить гусеницу от любого хищника в любое время, в особенности если хищник голоден. Идеальная стратегия состоит в том, чтобы быть как можно более незаметной. Некоторые гусеницы близки к этому идеалу, а при виде разнообразия и изощренности стратегий, используемые сотнями видов чешуекрылых, чтобы остаться незамеченными, невольно вспоминаются слова выдающегося натуралиста XIX в. Жан Луи Агассиса: «Экстравагантность настолько глубоко отражает самую возможность существования, что вряд ли найдется какая-нибудь концепция, которую Природа не реализовала бы как слишком экстраординарную»10.
Мы не можем удержаться от искушения привести пример, заимствованный у Милтона Лава11. Трематод (плоский червь), паразитирующий в печени овцы, проходит путь от муравья до овцы, где наконец происходит самовоспроизведение. Вероятность того, что овца проглотит инфицированного муравья, сама по себе очень мала, но поведение такого муравья изменяется самым удивительным образом, и вероятность, по-прежнему оставаясь малой, становится максимальной. Можно с полным основанием сказать, что трематод «завладевает» телом своего хозяина. Он проникает в мозг муравья и вынуждает свою жертву вести себя самоубийственным образом: порабощенный муравей вместо того, чтобы оставаться на земле, взбирается по стеблю растения и, замерев на самом кончике листа, поджидает овцу. Это — поистине «остроумное» решение проблемы для паразита. Остается загадкой, как оно было отобрано.
Модели, аналогичные логистическому уравнению, позволяют исследовать и другие ситуации, возникающие в ходе биологической эволюции. Например, такие модели помогают определить условия межвидовой конкуренции, при которой определенной части популяции выгодно специализироваться на «военной», непроизводительной деятельности (таковы, например, «солдаты» у общественных насекомых). Можно также указать, в какой среде специализированный вид с ограниченным диапазоном пищевых ресурсов имеет более высокую вероятность, выжить, чем неспециализированный вид, потребляющий более разнообразные пищевые ресурсы12. Но здесь мы сталкиваемся с некоторыми весьма различными проблемами организации внутренне дифференцированных популяций. Во избежание путаницы и недоразумений необходимо установить четкие «демаркационные линии». В популяциях, где отдельные особи различимы, где каждая особь наделена памятью, обладает своим характером и опытом и призвана играть свою особую роль, применимость логистического уравнения или, более общо, простого аналога дарвиновских идей становится весьма относительной. В дальнейшем мы еще вернемся к этой проблеме.
Интересно отметить, что кривая на рис. 21, показывающая, как последовательно сменяются при увеличении параметра К-т/r периоды роста и пики семейства решений логистического уравнения, может также описывать размножение некоторых технологических продедур или продуктов. Открытие или технологическое новшество, появление нового продукта нарушает сложившееся социальное, технологическое или экономическое равновесие. Такое равновесие соответствует максимуму кривой роста техники или продуктов производства, с которыми новшеству приходится вступать в конкуренцию (в ситуации, описываемой логистическим уравнением, они играют аналогичную роль13). Приведем лишь один пример. Распространение пароходов привело не только к почти полному исчезновению парусного флота, но и за счет снижения транспортных расходов и повышения скорости перевозок способствовало увеличению спроса на морской транспорт (т. е. увеличению параметра K), что в свою очередь повлекло за собой увеличение численности транспортных судов. Разумеется, ситуация, о которой мы говорим здесь, предельно упрощена и, по предположению, подчиняется чисто экономической логике: технологическое новшество в данном случае лишь удовлетворяет (хотя и иным путем) ранее существовавшую потребность, которая остается неизменной. Но в экологии и человеческом обществе имеется немало примеров инноваций, оказавшихся успешными, несмотря на отсутствие предварительной «ниши».
6. Эволюционная обратная связь
Мы сделаем первый шаг к объяснению эволюционной обратном связи, если будем считать «несущую способность» системы не постоянной, как это было до сих пор, а функцией того, как используется система.
Такое расширение модели позволит нам учесть некоторые дополнительные аспекты экономической деятельности, и в частности некоторые «эффекты усиления». Например, мы получаем возможность описать самоускоряющиеся свойства системы и пространственную дифференциацию различных уровней активности.
Географы уже построили модель, коррелирующую эти процессы. Мы имеем в виду модель Кристаллера, определяющую оптимальное пространственное распределение центров экономическом деятельности. Крупные городские центры располагаются в узлах шестиугольной решетки. Каждый из центров окружен кольцом городов следующего по величине масштаба, те в свою очередь окружены тяготеющими к ним еще меньшими населенными пунктами и т. д. Ясно, что в действительности такое геометрически правильное строго иерархическое распределение встречается очень редко: немало исторических, политических и географических факторов нарушают пространственную симметрию. Но рассматриваемая модель нереалистична и по другим причинам. Даже если бы мы исключили все наиболее важные источники асимметричного развития и начали с однородного в экономическом и географическом отношениям пространства, моделирование генезиса распределения, по Кристаллеру, приводит к выводу о том, что описываемая моделью статическая оптимизация является возможным, но маловероятным исходом эволюции.
Рассматриваемая модель[14] использует лишь минимальный набор переменных, входящих в вычисления, аналогичные, проведенным Кристаллером. Построено несколько уравнений, обобщающих логистическое. При выводе их авторы исходят из основного предположения о том, что способность населения мигрировать есть функция локальных уровней экономической активности, определяющих своего рода локальную «несущую способность», которая в данном случае сводится к занятости населения. Но местное население есть в то же время потенциальный потребитель товаров, производимых местной промышленностью. Таким образом, в локальном. развитии существует двойная положительная обратная связь, называемая «городским мультипликатором»: и локальное население, и экономическая структура, сложившаяся при уже достигнутом уровне активности, способствуют дальнейшему его повышению. Вместе с тем каждый локальный уровень активности определяется конкуренцией с аналогичными центрами экономической активности, расположенными в других местах. Сбыт произведенных продуктов или оказываемых услуг зависит от стоимости транспортировки их к потребителю и масштабов «предприятия». Расширение любых предприятий определяется спросом на то (товар или услугу), производству чего оно способствует и за производство чего данные предприятия конкурируют с другими. Таким образом, между относительным ростом населения и производительной деятельностью или сферой услуг существуют сильная обратная связь и нелинейные зависимости.
За исходное состояние в рассматриваемой модели приняты гипотетические начальные условия, при которых в различных точках наблюдается (сельскохозяйственная) активность «уровня 1″. Модель позволяет проследить возникновение иерархически упорядоченной активности, соответствующей более высоким уровням иерархии по Кристаллеру, т. е. подразумевающей экспорт произведенной продукции в более широкую область. Модель показывает, что даже если начальное состояние совершенно однородно, то одной лишь игры случайных (т. е. не контролируемых моделью) факторов, таких, как место и время закладки различных предприятий, достаточно для нарушения симметрии — появления зон с высокой концентрацией активности и одновременным спадом экономической активности в других областях и оттоком из них населения. Проигрывание модели на ЭВМ позволяет наблюдать расцвет и упадок, подчинение одного экономического центра другому и соответственно доминирование одних центров над другими, периоды, благоприятные для развития альтернативных направлений, и сменяющие их периоды «замораживания» уже существующих структур.
В то время как симметричное распределение Кристаллера игнорирует «историю», изложенный выше сценарий учитывает ее (по крайней мере самым минимальным образом) как взаимодействие «законов», имеющих в данном случае чисто экономическую природу, и «случая», управляющего последовательностью, в которой возникают предприятия.
7. Моделирование сложности
Несмотря на свою простоту, наша модель довольно точно передает некоторые особенности эволюции сложных систем. В частности, она проливает свет на природу трудностей «управления» развитием, зависящим от большого числа взаимодействующих элементов, Каждое отдельное действие или локальное вмешательство в систему обретает коллективный аспект, который может повлечь за собой совершенно неожиданные глобальные изменения. Как подчеркивал Уоддингтон, в настоящее время мы еще мало знаем о наиболее вероятной реакции системы на то или иное изменение. Очень часто отклик системы на возмущение оказывается противоположным тому, что подсказывает нам наша интуиция. Наше состояние обманутых ожиданий в этой ситуации хорошо отражает введенный в Массачусетском технологическом институте термин «контринтуитивный»: «Эта проклятая штука ведет себя не так, как должна была бы вести!» В подтверждение сошлемся на классический пример, приведенный Уоддингтоном: программа ликвидации трущоб вместо того, чтобы улучшить, еще более ухудшает ситуацию. Новые здания, построенные на месте снесенных, привлекают в район большее число людей, но если их занятость не обеспечивается, то они продолжают оставаться бедными, а их жилища становятся еще более перенаселенными15. Мы приучены мыслить в терминах линейной причинности, но теперь нуждаемся в новых «средствах мышления». Одно из величайших преимуществ рассмотренной модели состоит как раз в том, что она позволяет нам находить такие средства и разрабатывать способы их оптимального использования.
Как мы уже отмечали, логистические уравнения наиболее пригодны, когда критическим измерением является рост популяции, будь то популяция животных, совокупность их навыков или активностей. Логистическая модель исходит из предположения о том, что каждый член популяции может быть выбран и рассматриваться как эквивалент любого другого члена. Но эту общую эквивалентность надлежит рассматривать не как незыблемый факт, а лишь как приближение, достоверность которого зависит от связей, наложенных на популяцию, от оказываемого на нее давления и от стратегии, избираемой популяцией для того, чтобы противодействовать вмешательству извне.
Взять хотя бы различие, проводимое экологами между К-стратегиями и r-стратегиями (К и r — параметры, входящие в логистическое уравнение). Хотя это различие относительно, оно проявляется особенно отчетливо в дивергенции, обусловленной систематическим взаимодействием между двумя популяциями, в частности взаимодействием хищник — жертва. Типичной для популяции жертв эволюцией является увеличение рождаемости r, а для популяции хищников — совершенствование способов ловли жертв, т. е. увеличение коэффициента К. Но повышение К в рамках логистической модели влечет за собой последствия, выходящие за круг явлений, описываемых логистическими уравнениями.
Как заметил Стивен Дж. Гулд[16], К-стратегия подразумевает, что индивид все более повышает свою способность обучаться на опыте и хранить накопленную информацию в памяти. Иначе говоря, индивиды становятся все более сложными и со все более долгим периодом созревания и обучения. В свою очередь это означает, что индивиды становятся все более «ценными», представляющими более крупные вложения «биологического капитала» и уязвимыми на протяжении более продолжительного периода. Развитие «социальных» и «семейных» связей является, таким образом, логическим аналогом К-стратегии. С этой точки зрения другие факторы, помимо численности индивидов в популяции, становятся все более существенными, и логистическое уравнение, измеряющее успех по числу индивидов, все хуже отражает истинное положение дел. Перед нами достаточно наглядный пример, показывающий, почему к моделированию сложных явлений следует относиться с осторожностью: в сложных системах дефиниция самих сущностей и взаимодействия между ними в процессе эволюции могут претерпевать изменения. Не только каждое состояние системы, но и само определение си-темы в том виде, в каком ее описывает модель, обычно нестабильно или по крайней мере метастабильно.
Мы подходим к проблемам, в которых методология неотделима от вопроса о природе исследуемого объекта. Мы не можем задавать одни и те же вопросы относительно популяции мушек, рождающихся и погибающих миллионами без сколько-нибудь заметных признаков обучения на опыте или расширения опыта, и относительно популяции приматов, каждый член которой является как бы тончайшим переплетением собственного опыта и традиций популяции.
Нетрудно видеть, что и в самой антропологии необходим принципиальный выбор между различными подходами к коллективным явлением. Хорошо известно, например, что структурная антропология отдает предпочтение тем аспектам общества, к которым применимы средства и методы логики и конечной математики, а именно: к элементарным структурам родства или анализу мифов, трансформации которых нередко сравнимы с ростом кристаллов. Дискретные элементы подсчитываются и комбинируются. Такой комбинаторный подход в корне отличается от подходов, анализирующих эволюцию в терминах процессов, которые охватывают большие, частично хаотические популяции. Мы имеем здесь дело с двумя различными взглядами и двумя типами моделей: Леви-Строс называет их соответственно механической и статистической моделями. В механической модели «элементы того же масштаба, что и явления», а индивидуальное поведение основано на предписаниях, относящихся к структурной организации общества. Антрополог выявляет логику этого поведения, а социолог со своей стороны работает со статистическими моделями больших популяций и определяет средние и пороги17.
Общество, определяемое исключительно в терминах функциональной модели, соответствовало бы аристотелевской идее о естественной иерархии и естественном порядке. Каждое официальное лицо исполняло бы все то, что входит в круг его обязанностей. Эти обязанности осуществляют перевод различных аспектов организации общества как целого с одного уровня на другой. Король отдает приказы архитектору, архитектор — подрядчику, подрядчик — строительным рабочим. На каждом уровне имеется свой руководитель. В то же время поведение термитов и других общественных насекомых ближе к статистической модели. Как мы уже видели, при возведении своего «дома» термиты не следуют указаниям одного руководящего разума. Взаимодействие между индивидами порождает при некоторых условиях определенные типы коллективного поведения, но ни одно из этих взаимодействий не соотносится с глобальной задачей, все взаимодействия чисто локальны. Такое описание подразумевает обращение к средним и вновь поднимает вопрос относительно устойчивости и бифуркаций.
Какие события способствуют регрессу и какие прогрессу системы? В каких ситуациях перед системой возникает необходимость выбора и в каких ситуациях режимы стабильны? Поскольку размеры или плотность системы могут играть роль параметра бифуркации, как может чисто количественный рост приводить к качественно новому выбору? Для ответа на эти вопросы понадобилась бы обширная исследовательская программа. Как и в случае с r- и K-стратегиями, поставленные нами вопросы приводят к обоснованию выбора «хорошей» модели социального поведения и истории. Каким образом в ходе эволюции популяция становится все более «механической»? Параллелизм между этим вопросом и теми вопросами, с которыми мы уже сталкивались при рассмотрении биологических проблем, очевиден. Например, каким образом отбор генетической информации, управляющей скоростями и регулированием метаболических реакций, делает одни пути настолько наиболее предпочтительными, чем другие, что развитие кажется целенаправленным или напоминает передачу «сигнала»?
Мы полагаем, что модели, построенные на основе понятия «порядок через флуктуации», помогут нам справиться с подобными вопросами, а при определенных обстоятельствах будут способствовать более точной формулировке сложного взаимодействия между индивидуальным и коллективным аспектами поведения. С точки зрения физика, к этому кругу проблем относится проведение различия, с одной стороны, между состояниями системы, в которых всякая индивидуальная инициатива малозначима, а с другой стороны, между областями бифуркаций, в которых индивидуальная идея или даже новое поведение может порождать глобальное состояние. Но даже в областях бифуркации усиление — удел далеко не каждой индивидуальной идеи и не каждого индивидуального поведения, а лишь «опасных», т. е. способных обратить себе на пользу нелинейные соотношения, обеспечивавшие устойчивость предыдущего режима. Таким образом, одни и те же нелинейности могут порождать порядок из хаоса элементарных процессов, а при других обстоятельствах приводить к разрушению того же порядка и в конечном счете к возникновению новой когерентности, лежащей уже за другой бифуркацией.
Модели «порядка через флуктуации» открывают перед нами неустойчивый мир, в котором малые причины порождают большие следствия, но мир этот не произволен. Напротив, причины усиления малых событий — вполне «законный» предмет рационального анализа. Флуктуации не вызывают преобразования активности системы. Если воспользоваться образным сравнением Максвелла, можно сказать, что спичка может стать причиной лесного пожара, но одно лишь упоминание о спичке еще не позволяет понять, что такое огонь. Кроме того, если флуктуация становится неуправляемой, это еще не означает, что мы не можем локализовать причины неустойчивости, вызванной усилением флуктуаций.
8. Открытый мир
Ввиду сложности затронутых нами вопросов мы вряд ли вправе умолчать о том, что традиционная интерпретация биологической и социальной эволюции весьма неудачно использует понятия и методы, заимствованные из физики18, — неудачно потому, что они применимы в весьма узкой области физики и аналогия между ними и социальными или экономическими явлениями лишена всякого основания.
Первый пример тому — парадигма оптимизации. И управление человеческим обществом, и действие селективных «воздействий» на систему направлены на оптимизацию тех или иных аспектов поведения или способов связи, но было бы опрометчиво видеть в оптимизации ключ к пониманию того, как выживают популяции и индивиды. Те, кто так думает, рискуют впасть в ошибку, принимая причины за следствия, и наоборот.
Модели оптимизации игнорируют и возможность радикальных преобразований (т. е. преобразований, меняющих самую постановку проблемы и тем самым характер решения, которое требуется найти), и инерциалъные связи, которые в конечном счете могут вынудить систему перейти в режим функционирования, ведущий к ее гибели. Подобно доктринам, аналогичным «невидимой направляющей руке» Адама Смита, или другим определениям прогресса в терминах критериев максимизации или минимизации, модели оптимизации рисуют утешительную картину природы как всемогущего и рационального калькулятора, а также строго упорядоченном истории, свидетельствующей о всеобщем неукоснительном прогрессе. Для того чтобы восстановить и инерцию, и возможность неожиданных событий, т. е. восстаповить открытый характер истории, необходимо признать ее фундаментальную неопределенность. В качестве символа мы могли бы использовать явно случайный характер массовой гибели в меловой период живых существ, исчезновение которых с лица Земли расчистило путь для развития млекопитающих — небольшой группы крысообразных животных19.
Сказанное выше было лишь общим изложением, своего рода «видом с птичьего полета». Mы обошли молчанием многие важные вопросы (например, большой теоретический и практический интерес представляют неустойчивости, возникающие в пламёнах, плазме и лазерах в сильно неравнонесных условиях). Всюду, куда бы мы ни бросили свой взгляд, нас окружает природа, неисчерпаемо разнообразная и щедрая на всякого рода новаторские решения. Описываемая нами концептуальная эволюция сама по себе является лишь составной частью более широкой истории последовательного, шаг за шагом переоткрытия времени.
Мы видели, как физика постепенно обогащалась все новыми и новыми аспектами времени, между тем как присущие классической физике претензии на всемогущество одна за другой отпадали как необоснованные. В этой главе мы шли от физики через биологию и экологию к человеческому обществу, хотя могли бы двигаться и в обратном направлении: история занималась изучением в основном человеческих сообществ и лишь затем распространила свое внимание на временные аспекты жизни и геологии. Таким образом, вхождение времени в физику явилось заключительным этапом все более широкого «восстановления прав» истории в естественных и социальных науках.
Интересно отметить, что на каждом этапе этого процесса наиболее важной отличительной особенностью «историизации» было открытие какой-нибудь временной неоднородности. Начиная с эпохи Возрождения западное общество вступало в контакт со многими цивилизациями, находившимися на различных этапах развития; в XIX в. биология и геология открыли и классифицировали ископаемые формы жизни и научились распознавать в ландшафтах сохранившиеся до нашего времени памятники прошлого; наконец, физика XX в. также открыла своего рода «ископаемое» — реликтовое излучение, поведавшее нам о «первых минутах» Вселенной.
